基因组拷贝数目变异(CNV)临床诊断分析应用项目商业计划书
(讨论稿)
目录
什么是基因组拷贝数目变异(CNV)
国际国内CNV应用局限性和主要存在的问题
项目组在CNV临床检测的技术实力和目标
核心团队
潜在市场
资金需求
盈利计划
风险评估
风险控制
![]()
基因组拷贝数目变异(CNV)
基因组拷贝数异常(copy number variations,CNV)是属于基因组结构变异,根据大小可分为两个层次:显微水平和亚显微水平。显微水平的基因组结构变异主要是指显微镜下可见的染色体畸变,包括整倍体或非整倍体、缺失、插入、倒位、易位、脆性位点等结构变异。亚微水平的基因组结构变异是指DNA片段长度在1Kb以上的基因组结构变异,包括缺失、插入、重复、重排、倒位、DNA拷贝数目变化等,这些变化将导致位于该区域内的基因表达量受到严重影响。

上图:正常人类基因组构成成分是等位基因成对存在的,当基因组出现缺失或重复时候,导致拷贝数量的变异(CNV) 。
CNV的临床意义和应用领域
CNV是遗传疾病研究和诊断的新方向:2004和2012年美国哈佛大学医学院和加拿大儿童医学基因组应用学研究中心CNV领域的两篇奠基之作,(1.在人类基因组上发现大片段变异。2.人类基因组上的大片段拷贝数多态性)分别发表在自然(Nature)杂志与科学(Science)杂志,从此开启了解开人类基因组奥秘的新探索,研究人员和医疗机构开始进行相关的科学和临床关联研究。目前已经证实CNV在人类基因组的广泛存在,从数百个碱基对(bp)到数百万bp范围内都存在有缺失、插入、重复和复杂的多位点变异。同时多个研究表明CNV与人类复杂的遗传疾病有着紧密的联系,可导致不同程度的受累基因表达异常,是相关人类疾病的重要原因。CNV的研究不仅有助于解释为什么复杂疾病往往是遗传获得的,但并不总是和同一基因关联。CNV将随机个体之间的基因组差异估计值提高到大于1%,大大改变了人们先前的认识,正在改变人类对遗传学领域的认知。不同的CNV可导致不同基因、不同程度表达差异,对正常表型的构成及多种疾病的发生发展具有重要作用,CNV特别是对于复杂疾病的诊断和表现型多样性的解释具有重要意义。
1.
CNV的发生会对人类健康影响更严重:与一直以来研究较多的单核苷酸多态性(SNPs)和病理性的单核苷酸变异相比,CNV发生的频率虽偏低,但累及的序列长度、基因数目、核苷酸数目却明显超过了前者,对基因组的影响比起SNP更大,一旦发生往往会给生命体带来重大缺陷,对人类健康和疾病的影响更为显著。将可能导致导致严重出生缺陷、癌症等。比如严重的脑病、心肌病、肌病、白血病、家族性遗传性结肠癌息肉病等等多种重大疾病,都和基因组的结构性变异直接相关。
2.
CNV是明确部分新的原发性疾病的重要手段:CNV具有很高形成速率,是多种新的未知疾病的发生原因。CNV的形成与众所周知的非同源末端连接,以及新近提出的DNA复制扰动和不连续DNA复制有关。多种机制共同作用,原发性CNV的形成速度远远超过其他类型的基因变异,导致一些新型疾病、疑难疾病、多系统交叉疾病的出现,CNV是明确这些疾病的重要手段。
3.
CNV是产前重大遗传病和家族性遗传疾病的预防诊断必不可少的:人类已知的染色体疾病有数百种之多。大片段CNV异常,统称为染色体微缺失/微重复综合征,这种大片段的DNA缺失或者重复是严重染色体疾病的主要原因,全基因CNV检测对产前诊断和产后家族性基因异常的评估,优生优育等具有重要意义。
4.
CNV是多学科多种疾病发生的重要原因:不仅严重的染色体异常如微缺失/微重复综合征与CNV密切相关,同时大量小片段的CNV或者累及单基因的CNV也是很多疾病的致病原因。CNV可存在于所有23对染色体中的任一或者多个、在全基因组的任何区域均可发生,可能涉及单个基因或者多个基因,可累及致病基因或者非致病基因,也可以是小片段或者大片段或者累及整个染色体长臂或者短臂,因此,CNV的类型多种多样,千变万化,导致疾病的多样化。
不同区域的CNV可造成不同的机体功能异常,致病性的CNV可导致人体器官先天异常(例如先天畸形、肢体残疾、发育迟缓、智力障碍)、多种关键酶学缺陷、多种神经系统疾病(例如PWAS综合征,多种肌病)、心血管系统疾病(例如肥厚性心肌病、致命性的长QT综合征)、免疫系统疾病(例如免疫缺陷综合征)、线粒体系统(例如眼外肌萎缩等等)、以及多种肿瘤(HNPCC遗传性结肠癌、胰腺癌)等数百种疾病发生等等。各个医学学科中大量的遗传疾病、诊断不明的疾病可能由于CNV的存在而造成,急需要从基因水平提供明确的诊断依据和为治疗方案的选择提供参考。
国际国内CNV应用局限性和主要存在的问题
1.
应用领域的片面性:目前在国内只有极为少数具有技术条件和资质的医疗机构和公司进行CNV的研究和临床应用,主要应用在儿童复杂罕见遗传病、自然流产新生儿死亡等妊娠常务的遗传学检测、产前诊断核型异常的进一步异常分析,应用范围局限,积累的经验少。事实上,CNV的存在是人类的很多疾病的原因,包括多种肿瘤(结肠癌、肺癌、胰腺癌、内分泌肿瘤、颅内肿瘤等)、罕见疾病、多种神经系统疾病、多种心血管疾病、多种代谢疾病,线粒体疾病的CNV检测在国内尚未有效开展,亟待开发并应用于临床多学科。
2.
检出率的低下:不同的CNV检测平台和基因芯片的分辨率会造成同一样本得出不同的检测结果。目前的国内采用的方法主要是低分辨的基因芯片,因此造成很多有意义的病理性的CNV不能检测,例如一般公司基因的检测精度在5KB大小的缺失和重复,事实上,在人类基因组不仅存在大片段的CNV,同样也存在大量的小片段CNV涉及到单个基因和单个基因的外显子,这些也是造成疾病的重要原因。由于技术和仪器精度的不够使得这个片段被大量错失不能检出。另外也有大量的病理性CNV起始点和终止点存在于基因内含子,常规方法都不能够检测到,从而造成大量的漏诊和误诊。目前国内仅有极少数公司开展CNV相关的检测,但都存在低精度的问题。
3.
检测结果的验证缺乏规范化。新技术的发展、成熟和应用,必然会对临床体系产生巨大影响。目前在国内临床CNV诊断的实践中,各级医务人员没有统一的认识来如何正确定适宜的临床适应症,对CNV技术的临床使用中的技术路线、遗传咨询、应用规范、差异性结果的判定以及临床研究方向,都是亟待解决的重大课题。
4.
检测结果判读能力缺乏:对CNV判读能力的不足时困扰分析人员的最大问题,也是造成在国内CNV应用受到限制的主要原因,如果不能正确和全面的判读检测结果,将不能为临床提供有效和精确的诊断。对于罕见的新生CNV,嵌合体CNV、不同外显率CNV的判读和解释依然非常困难。后面部分将对本项目团队在这方面的优势和经验做进一步的阐述。
国际学术界解读CNV临床意义的难点
随着CMA、CNV-seq、WES、WGS等高分辨率技术应用于人类基因组CNV检测,临床上检测出大量的CNV片段。对于如何解读检测出的CNV临床意义,长期困扰着临床医生和基因检测机构。基因变异的解读作为遗传咨询工作中重要组成部分,也是最具有挑战性的工作,在我们基因变异的解读仍然是面临的重大问题。
1.
缺乏科学完善可靠的判读标准:国际学术界而言,CNV解读流程都是参考CNV与人群多态性数据库、微缺失/微重复综合征数据库、基因组异构数据库、网络数据库、文献中报道以及是否包含重要功能性基因等来确定临床意义。2015年美国遗传病协会ACMG发表一个初步简单的CNV临床意义分析指南,基因CNV变异的解读基本都是基于这个指南,但它是很不完善一种框架化的指导,但只是一个方向性的指导,可操作性弱,对于CNV重复和复杂的CNV的解读并不适应,无法满足特定的临床环境。
2.
判读结果的误差和不一致:近期的研究表明,即使使用相同的解读框架,不同实验室的病理学家也存在分歧,甚至在某些情况下,对于同一个变异的致病性,不同机构会有着截然不同的结论。在2016年美国分子病理学会(AMP)年会上,研究人员曾分享了来自于AMP工作小组名为“VITAL项目”的早期研究数据,该计划旨在揭示不同实验室对于相同遗传变异的解读存在差异的确切原因。结果显示,即使AMP采用使变异解读更统一的策略或依据指南,差异也仍然存在。
3.
人类CNV结构的复杂性与多样性:人类可能存在的CNV达数万种之多, CNV可存在于人类基因组中任何区域,大小尺寸、累及区域、受累基因、受累功能基团等都可能不同,形式多种多样,导致疾病的临床表现型千变万化。同时,不同的CNV也可能出现相同临床表现型,不仅已经检测到很多致病性的CNV存在,同时也存在大量非致病性的CNV。因此,区分致病与非致病CNV,正确评估CNV基因型与表现型的关联这些结果判读中的难点。
4.
个性特征、遗传方式的复杂性:由于CNV致病性的分析是非常复杂的过程,需要考虑许多证据、个性特征以及了解证据的复杂性,目前在制定完整而全面的评判标准非常困难,各基因诊断机构都缺乏正式和完整的判定标定。在一个缺乏标准化的领域中,难免会遇到定义模糊的问题,在评估指标、疾病关联等方面急需要细化和拓展。
5.
大量无效基因和多态性CNV的干扰。基因组结构中也存在大量假基因、非转录基因,这些无效基因会对CNV和正常编码基因的拷贝数目的判定与意义的评估带来强烈的干扰。大量的多态性CNV和非致病性CNV的存在导致部分新发现CNV不能够给出准确和正确的病理学分类,只能给与一个模糊和的不明确临床意义的结论。
由于上述种种因素的存在,CNV的解读是目前本领域最困难和最具挑战性的。本项目正是针对这种国际国内一直面临的困局开发一种前沿性的解决方案或建立一种新型评判量化标准。
项目组在CNV临床检测的技术实力和目标
目前美国三大临床检验公司(LabCorp,Quest,Bioreference),目前,只有Bioreference旗下的基因诊断公司从2019年初开始尝试采用WGS进行CNV检测,但也属于初始阶段。我们期待利用本项目的技术实力所长,奠定在CNV检测和评判方面的行业技术优势,并协助带动和提高中国基因CNV诊断水平到一个新的高度。
1.
优势高端技术人才:团队技术高管曾经作为教授、主任医师、研究生导师在中国顶级医疗机构解放军总医院进行临床、科研和教学多年,不仅具有在中国的丰富临床经验和医疗资质。同时作为首席技术科学家、项目经理、技术主管等在美国著名大学医学院、科研机构、基因诊断公司从事20多年的分子生物和遗传诊断研究、临床、科研和教学,在临床医学、遗传研究、基因诊断领域积累了丰富的经验。具备有足够分子诊断技术实力实施国际一流水准的全面而准确的基因诊断服务。
2.
采用世界最先进的高通量CNV检测设备:使用与美国类似项目的同步使用技术和设备,保持国内类似项目的领先实验室水准进行CNV检测。
3.
项目组已成功完成多个大型数据库的整合:可为CNV结果的判读提供可靠的依据和保障。
4.
领先的CNV相关分析技术:本项目组团队掌握并独创了多种与基因突变分析相关的技术,希望在未来通过我们的努力将这些分析方法应用到CNV的临床意义的评定方面,并制定了一整套属于本项目独特和独有的CNV致病性的量化指标与评判标准,包括单基因疾病和多基因疾病的致病意义的标准,这将对提高诊断评判的一致性,对临床致病性分析具有重大的意义,而且可为临床提供准确而又具有诊断和指导意义的检验结果报告。
5.
创立CNV病理学意义评估知识体系成果:团队成员在美国Lombardi肿瘤中心分子与遗传研究所建立和发展线粒体基因诊断等多项分子技术、为美国纽约Downstate医学中心建立基因诊断临床实验中心,在美国最大基因检测诊断公司开展了美国及全球临床检测诊断业务,具有基因组拷贝数变异(CNV)检测与病理学意义评估诊断标准的大量经验及知识体系成果,在经验积累的基础上已经基本完成本项目独有的大尺度CNV和小片段CNV,多基因和单基因CNV的全面的、科学的、可操作的解读量化指标评估系统,形成了成熟可靠的可以直接引进产业体系应用于中国人群的疾病基因诊断,有效弥补国内在这方面的空白和缺陷。
6.
项目组团队优势:本项目的核心团队成员包括四方面的人才层次:一是具有国际前沿水准的全基因CNV诊断分析领域的教授级专家;二是具有大型健康项目管理和国际大型金融机构工作经验的项目管理型专家;三是具有涉及基因领域的临床分子遗传疾病和疑难杂病医学专家,提供直接的临床医学指导;四是具有国内企业上市、并购重组、财务顾问等业务的实际操作经验的经济学专家。在核心团队成员的基础上,医学专家群汇集了全国各学科专家和优秀医疗资源。基于项目需要,本项目还有还更多的医学领域资源可以请各个医学领域的专家教授给予指导。
本项目的前沿性和开拓性内容概要:
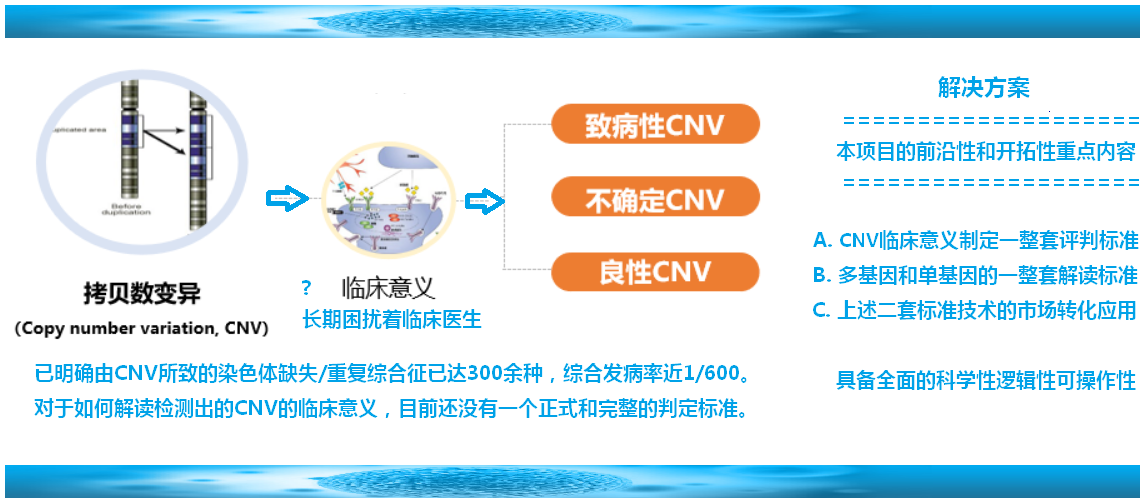
在短时间内开创一个满足人民健康需要的应用型新产品--CNV标准化疾病诊断分析工具;通过这种新型诊断工具的实际应用,开拓全国的下一代基因临床诊断分析的全新市场,使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。
核心团队
本项目的核心团队成员包括四方面的人才层次:一是具有国际前沿水准的全基因CNV诊断分析领域的教授级专家;二是具有大型健康项目管理和国际大型金融机构工作经验的项目管理型专家;三是具有涉及基因领域的临床分子遗传疾病和疑难杂病医学专家,提供直接的临床医学指导;四是具有国内企业上市、并购重组、财务顾问等业务的实际操作经验的经济学专家。在核心团队成员的基础上,将通过吸收、招聘和培训等方式,建立起项目执行团队,完成项目的开展与实施。
项目协作单位/医学领域医疗顾问名单:
。。。。。
(注:医学专家群汇集了全国各学科专家和优秀医疗资源。基于项目需要,本项目还有更多的医学领域资源可以请各个医学领域的专家教授给予指导。)
潜在市场
国际上,麦肯锡发布了一项报告,里面研究了技术对未来经济影响程度。研究的对象是一些正在取得飞速发展、具有宽泛影响,且对经济影响显著的技术。下一代基因组学位于第七,经济:0.7─1.6万亿美元。生活:通过快速疾病诊断、新药物等延长及改善75%的生命。


国内而言,未来5-10年在数百亿至数千亿的规模。
资金需求
第一期(第一年) 融资需求
2000 万元人民币,主要用于:
1.组建公司、办公场地及设施:
120 万。
2.建立与美国类似项目同步使用技术和设备的临床检测实验室:1500
万。
3.人员:280
万。
第一年公司员工预设为8人,其中: 技术高管(1人);项目高管(1人);财经高管(1人);专业医生(1人);技术人员(2人);办公人员(2人)。
4.其它:100 万。

第二期(第二年) 融资需求
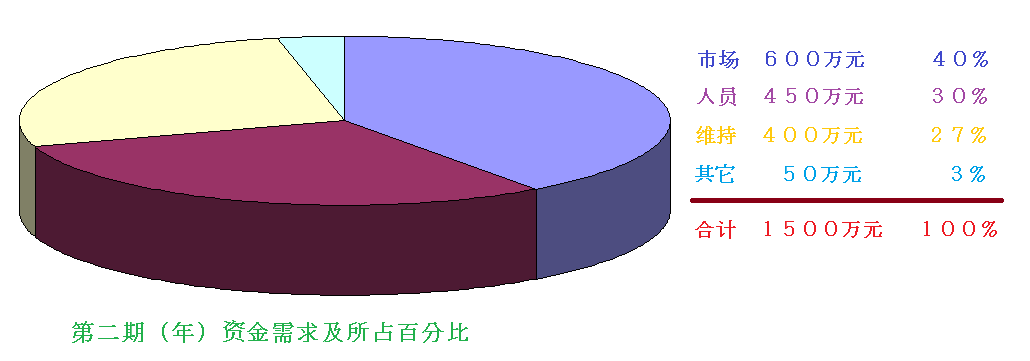
1500 万元人民币,主要用于:
1.市场开发:
600万。 (第一年节余部分可以考虑投入到市场开发中去)
2.办公场地及实验室维持业务运转的费用:
400 万。
3.人员:450
万。
第二年公司员工预设为16人,其中:技术高管(1人);项目高管(1人);财经高管(1人);专业医生(2人);技术人员(4人);办公人员(3人);市场营销(4人) 。
4.其它:50
万。
(注:因为市场的开发及增添能开展其它基因检测业务的设备及人员。项目也有可能开始部分创收。)
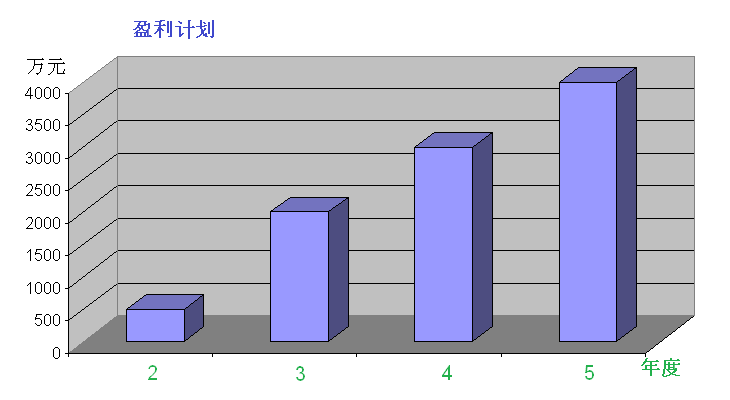
第三年及其以后:
实现盈利预期(盈利计划)
盈利计划
以本项的应用型新产品--CNV标准化疾病诊断分析工具--可以使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。这个诊断工具是本项目有知识产权性质和强大竞争力的核心产品。
项目建设周期预期为二年,第三年预期盈利,第四年预期回收投资总额,第五年预期纯盈利达4000--6000万水平的规模。
盈利估测 (全基因检验诊断分析)
|
|
保守性预估 |
平均性预估 |
实验室设计量 |
|
检验样本数(例/天) |
20 |
40 |
60 |
|
检验样本单价(元/例) |
10,000 |
10,000 |
10,000 |
|
全年有效开放天数 |
360 |
360 |
360 |
|
总营业收入 |
72,000,000 |
144,000,000 |
216,000,000 |
|
营业回报率 |
30% |
30% |
30% |
|
纯盈利收入 |
21,600,000 |
43,200,000 |
64,800,000 |
实验室开始运转的保守性预估:总营业收入在7千万左右规模,纯盈利收入在2千万左右规模。
实验室中期运转的平均性预估:总营业收入在1.4亿左右规模,纯盈利收入在4千万左右规模。
实验室设计量的平均性预估:总营业收入在2.1亿左右规模,纯盈利收入在6千万左右规模。
保守估计:
以保守平均每天20个检测样本,每个样本10000元人民币预计(注:基于美国已经开展的项目按国内情况估算),一年的产业规模就可达到7000万以上,其中,纯利润以30%计可达2100万。保守的每天20例样本预估是基于下列二种方式的市场必需可能性评估:
1.检测样本中,如果按病症来源可以估计如下:
肿瘤早筛:10-15例/每天(全年3650-5475例)
生育健康:6-8例/每天(全年2190-2920例)
少见病症:2-3例/每天(全年730--1095例)
复杂病症:2-4例/每天(全年730--1460例)
2.检测样本中,如果按送检来源可以估计如下:
来自全国医疗机构(约2万家):10-20例/每天(全年3650-7300例)
直接面向顾客方式(大众人群):10-20例/每天(全年3650-7300例)
3. 纯利润以30%计是基于下列考量:
2016年,华大公司实现营业收入17.1亿元,净利润5.87亿元,33.9%净利润率。(含非归属口利润2.37亿元)
2016年,贝瑞和康公司实现营业收入9.2亿元,净利润2.9亿元,31.5%净利润率。(含非归属口利润1.4亿元。)
具体计划:
第一年:组建公司并建立国际一流水准临床检测实验室及诊断评判新标准。
第二年:开展国内尚未开展的基因组拷贝数目变异(CNV)临床和非临床应用的新型业务。
第三年:建立和扩大业务市场,纯盈利预期不低于2000万元人民币。(以保守的平均每天20例样本的检测诊断计)
第四年:扩大市场,纯盈利预期不低于3000万人民币。(以平均每天30例样本的检测诊断计)
第五年:扩大市场,纯盈利预期不低于4000万人民币。(以保守的平均每天40例样本的检测诊断计)
其后:建立实验室其它分中心,期望下一个5年计划中保持20%的纯盈利收入增长速度。考虑项目更长远的规划,包括科研开发、更多服务项目开发和企业上市等等事项的布局。
具体计划中的考量是基于下列国内市场和行业参考数据:
国内三大上市医学独立实验室2018年营业情况:
|
企业名称 |
净利润(万元) |
同比上长 |
|
迪安诊断 |
32,963 |
49.53% |
|
金域医学 |
19,053 |
34.60% |
|
达安基因 |
10,158 |
17.51% |
(国内三大上市医学独立实验室2018的净利润都过亿,并且同比上长平均在30%以上。)
实际可能:
基因组拷贝数变异(CNV)诊断水准提升到国际水准上是医学临床和非临床的生物基因诊断未来发展方向和趋势所在,很大程度可以更充分开发其应用市场,并达到可观的盈利(实际达到产业规模上亿的可能性很大)。
1.随着中国中产阶层和富裕人群数量的增长,人们对自身健康和健康生活质量的重视程度也将相应更多的关注,而更新更广更精确的疾病筛查的诊断技术和能力也将在这些方面显示其市场需要性,而本项目的新型基因检测和诊断方法则是满足这种市场需要的时机点,相应的市场需求会越来越大。
2.肿瘤基因测序特别是早期肿瘤筛查──液体活检领域是基因测序领域下一个最有希望的「杀手级应用」和投资重点,其潜在市场空间远大于生育健康类服务。
3.一方面,基于精准医疗和现代健康管理模式,具体市场开发计划将会是多种形式;另一方面,基于人工智能和大数据时代,将导致或带来新的市场机遇。
4.开阔国际视野和市场,提前布局,国际多方多平台合作共赢市场模式也将是未来趋势。
风险评估
投资风险主要体现在下面几个环节:
1.政策上的风险:主要包括国家对人类基因学研究与应用的限制性变化。例如,
1)相关资质的申请和获得政府批准:包括营业执照,检验许可证,检测中心实验室建设需符合国家标准。
2)检验许可所需的前期临床试验报告,需要获得CFDA审批。
3)前期试验和CFDA审批过程时间长,需要一年甚至更长时间。
2.市场上的风险:主要可能是如何开发市场的方面,需要让临床医务人员认识到新知识体系和新技术体系相结合的新型诊断标准工具如何能更好地服务于临床上,才能竞争更多的市场。
3.技术上的风险:生物技术发展相当快,这是今后我们的项目可能面临被超赶的风险。
风险控制
1.政策上:国际和国内的基因行业的法规和政策是趋于越来越开放,要把握好这种趋势来开拓相应的市场;本项目组项目管理团队深刻认识到这些,也清楚明白相关管理部门的管理方式,尽早避免这类风险。
2.市场上:在市场开拓上,多作调查研究,了解市场可能的真正难点和解决之道,及时调整市场开发策略,选择成本效果的方式进行市场开发和竞争。
3.技术上:在保持本项目已有的优势情况下,注重未来新的发展,及时更新知识和技术体系;注重吸收新的人才和更新必要的仪器设备;创建科研形式的实验研究项目,鼓励创新和专利发明。
4.其它:
1)做好前期融资工作。注重寻求当地政府的政策和财政支持。注重融资方面的潜在投资人或单位。
2)严格按国家标准建设实验室和安排有专业资格的岗位人员。
3)充分发挥和利用专业团队已有专业技术方面的知识和能力。一个项目的成功,主要取决于技术和管理二方面,项目组将着重于这二方面,以建成国际前沿水准的实验室而努力。
总体而言,只要建成最新WGS技术的国际一流水准临床检测实验室并可以开展业务,就达到了预期的初步目的,这种新的前沿性的下一代实验室服务实体的形成,具有市场竞争优势,可以进一步融资和/或开展其它合作机会。
以本项在短时间内可以建成一个满足人民健康需要的应用型新产品--CNV标准化疾病诊断分析工具--就可以使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。从成本效益的角度,国际一流水准临床检测实验室的建成也就足够可以补偿前期的资金总投入。
![]()
项目计划书基本内容版本
基因组拷贝数目变异(CNV)临床诊断分析应用项目商业计划书
项目名片
目录
第一部分 项目背景
生物基因学检测应用项目的产业相关背景
中国政府的产业相关政策支持
基因组拷贝数异常(CNV)的相关问题
基因组拷贝数异常(CNV)正在解开人类基因组的奥秘
CNV基本概念
CNV的临床意义和应用领域
全基因组WGS分析替代一般基因检测的必要性
国际国内CNV应用局限性和主要存在的问题
国际学术界解读CNV临床意义的难点
项目组在CNV临床检测的技术实力和目标
全基因组测序WGS进行CNV检测的主要优势
拟采用的主要技术与设备
基因组拷贝数目变异(CNV)临床检测项目市场行业定位
基因组拷贝数目变异(CNV)临床检测项目市场现状
基因组拷贝数目变异(CNV)临床检测应用的目标客户
基因组拷贝数目变异(CNV)相关法律与监管方面
第二部分 项目实施
项目目标
项目策略
核心团队
项目协作单位/医学领域医疗顾问名单
拟开展的CNV和基因变异检测项目
实施计划
初期市场和营销
成本效益
盈利计划
资金需求
股份和股权
风险评估
风险控制
第三部分 附件
1. 市场和客户相关报告
国内主要基因公司及医学独立实验室企业的市场现状
刚需产品调研及非刚需产品调研
2.拟开展的CNV和基因变异检测项目
3. 项目核心团队人员简历
4.深圳政府有关促进企业发展的政策支持
项目名片
|
企业定位: |
民营高新生物基因技术和应用(医学类) |
|
|
|
|
企业目标: |
中国新型基因诊断标准化实用化(国际一流水准) |
|
|
新型基因检测和诊断实验室(国际一流水准) |
|
|
|
|
核心团队: |
美国基因检测和诊断技术专家 |
|
|
加拿大公共健康管理项目专家 |
|
|
美国分子遗传疾病疑难疾病医学专家 |
|
|
中国财经和企业管理专家 |
|
|
|
|
核心技术: |
基因诊断标准科学性量化实用化的知识体系(知识产权性质) |
|
|
基因前沿检测和诊断技术 |
|
|
|
|
主要市场: |
医学临床和非临床的生物基因诊断未来发展方向和趋势所在 |
|
|
|
|
产业规模: |
每年上亿规模的新型生物基因检测和诊断服务业 |
项目优势:
本项目的优势是高端专业人才具有美国多年的基因组拷贝数变异(CNV)诊断研究经验及知识体系,通过实施本项目,将建成一个国际一流水准的新型基因检测和诊断实验室,将前沿性和开创性地形成一个成熟可靠的自主原创性成果的产业体系。
本项目的最大的贡献将是把中国基因组拷贝数变异(CNV)临床应用层次提高到国际水准的行列,创建和提供一个基因组拷贝数目变异(CNV)临床检测的国际一流服务水准平台,更好地满足人群基因诊断相关服务的需要。
本项目的前沿性和开拓性内容概要:

在短时间内开创一个满足人民健康需要的应用型新产品--CNV标准化疾病诊断分析工具;通过这种新型诊断工具的实际应用,开拓全国的下一代基因临床诊断分析的全新市场,使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。
第一部分 项目背景
生物基因学检测应用项目的产业相关背景
基因检测(Genetic Test):
是从染色体结构,DNA序列,DNA变异位点或基因表现程度,提供受检者与医疗研究人员评估一些与基因遗传有关的疾病、体质或个人特质的依据,也是精准医学分析的一种方法。每一个人的DNA基因都是独特的个人化资讯,造成每一个人的先天体质,健康状况,特征都不相同。
一方面,尽管基因检测领域还处于新兴产业之中,但中国现有的单核苷酸变异的基因检测技术和相关应用已经开展,竞争激烈。另一方面,中国在新兴的基因组拷贝数目变异(CNV,以下简称CNV)临床检测应用却相对落后,许多方面甚至没有开展或处于空白状况,面临急待提高局面。
基因组学应用行业属于发展最快的高科技行业之一,以美国为代表的基因组拷贝数目变异(CNV)临床检测应用已经开展,开辟了一个新兴的基因诊断服务市场,也正在完善和形成一个新的基因组CNV检测标准。
2019年科技部部长万钢表示,与建设世界科技强国的伟大目标、国家经济社会发展的战略需求和当前生物技术迅猛发展的国际态势相比,中国生物技术发展还存在着自主原创性成果少,关键核心技术仍受制于人,技术转化效率低,产业化发展能力不足,生物战略资源保护和利用不够等问题。
本项目的优势是专家型高端人才具有美国多年的基因组拷贝数变异(CNV)诊断研究经验及知识体系,开发项目的理论和技术起点就是直接从国际前沿水准起步,将在国内前沿性和开创性地形成成熟可靠的自主原创性成果的产业体系。本项目的最大的贡献将是把中国基因组CNV临床应用层次提高到国际水准的行列,创建和提供一个基因组CNV临床检测的国际水准服务平台,更好地满足人群基因诊断相关服务的需要。


中国政府的产业相关政策支持
2015年,中国科技部成立了中国精准医疗战略专家组和国家精准医疗战略专家委员会,并计划2030年前在基础研究和应用研究方面投入600亿元,至此,精准医疗在中国已经上升为了“国家战略”。
2015年,国家卫计委发布《关于产前诊断机构开展高通量基因测序产前筛查与诊断临床应用试点工作的通知》,“无创产前基因检测”重新启动,试点产前诊断机构可择优与承担高通量基因测序检验试点任务的医疗机构建立合作关系。
2017年5月,科技部制定了《“十三五”生物技术创新专项规划》。提到,发展新一代基因测序技术,重视单分子技术的应用和测序数据的分析解读;发展单细胞分离、基因组扩增、转录组扩增和单细胞基因组分析技术;发展基因和蛋白质精准测量技术,推动生物检测技术向微量、痕量、单分子、高通量等方向发展。
2018年由科技部牵头,发改委、财政部共16部委组成的《国家生物技术发展战略纲要》编制;要凸显国家战略意志,中长期布局,超前部署谋划,引领跨越发展。同时,要技术创新与体制机制创新双轮驱动,开放融合发展。
在国家的相关政策支持持续加码的利好行业长期发展情况下,中国生物技术发展步入战略机遇期,开发基因组拷贝数目变异(CNV)临床检测应用的项目正处于这么一个有利的时期。
基因组拷贝数异常(CNV)的相关问题
自从上世纪80年代基因检测遗传病研究开始以来,基因检测疾病取得了长足的发展,特别是人类基因组计划完成之后,基因组医学的迅猛发展,一批人类疾病相关的基因被揭示而后迅速用于了疾病的风险评估、预防、诊断和治疗,对人类的健康起到了不可替代的作用。近年来,随着深度测序技术的发展和应用,更多的遗传病和恶性肿瘤的基因诊断得到了迅速的推广和应用。
基因组检测(genomic testing)是遗传学中一个较新的领域,它指的是对一个生物体的全部基因组(构成生物体的基因)进行观察的过程。与基因检测(genetic testing)只对某个特异基因或特定的基因组进行观察有所不同,基因组检测对遗传密码里任何的基因改变或有害变化进行广泛的测试。
基因组拷贝数异常(CNV)正在解开人类基因组的奥秘
CNV基本概念
基因组拷贝数异常(copy number variations,CNV)是属于基因组结构变异,根据大小可分为两个层次:显微水平和亚显微水平。显微水平的基因组结构变异主要是指显微镜下可见的染色体畸变,包括整倍体或非整倍体、缺失、插入、倒位、易位、脆性位点等结构变异。亚微水平的基因组结构变异是指DNA片段长度在1Kb以上的基因组结构变异,包括缺失、插入、重复、重排、倒位、DNA拷贝数目变化等,这些变化将导致位于该区域内的基因表达量受到严重影响。
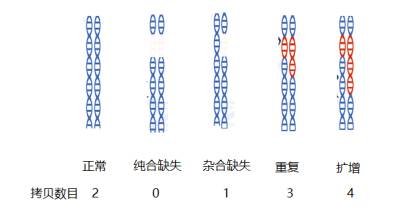
上图:正常人类基因组构成成分是等位基因成对存在的,当基因组出现缺失或重复时候,导致拷贝数量的变异(CNV) 。
CNV的临床意义和应用领域
1.
CNV是遗传疾病研究和诊断的新方向:2004和2012年美国哈佛大学医学院和加拿大儿童医学基因组应用学研究中心CNV领域的两篇奠基之作,(1.在人类基因组上发现大片段变异。2.人类基因组上的大片段拷贝数多态性)分别发表在自然(Nature)杂志与科学(Science)杂志,从此开启了解开人类基因组奥秘的新探索,研究人员和医疗机构开始进行相关的科学和临床关联研究。目前已经证实CNV在人类基因组的广泛存在,从数百个碱基对(bp)到数百万bp范围内都存在有缺失、插入、重复和复杂的多位点变异。同时多个研究表明CNV与人类复杂的遗传疾病有着紧密的联系,可导致不同程度的受累基因表达异常,是相关人类疾病的重要原因。CNV的研究不仅有助于解释为什么复杂疾病往往是遗传获得的,但并不总是和同一基因关联。CNV将随机个体之间的基因组差异估计值提高到大于1%,大大改变了人们先前的认识,正在改变人类对遗传学领域的认知。不同的CNV可导致不同基因、不同程度表达差异,对正常表型的构成及多种疾病的发生发展具有重要作用,CNV特别是对于复杂疾病的诊断和表现型多样性的解释具有重要意义。

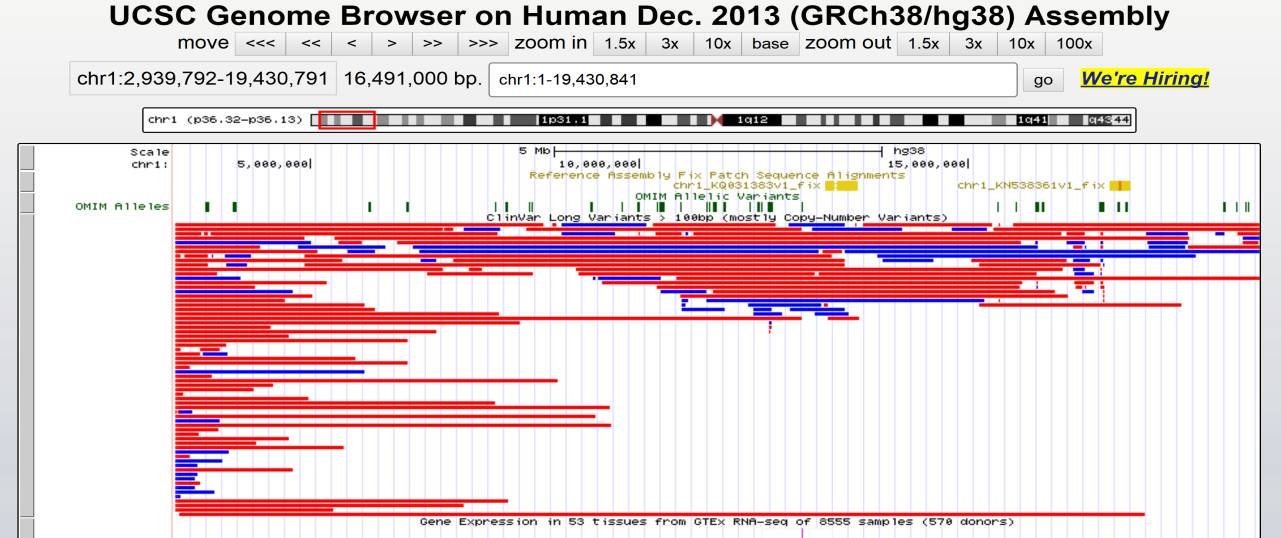
图1,已发现的CNV与染色体位置关系,http://projects.tcag.ca/variation/),其中染色体倒位847;100bp~1Kb的插入缺失为30748个;倒置断裂位点约14478个。此外,据研究估计,CNV至少占到基因组的12%,已成为基因组多态性和致病性原因的又一重要来源。
2.
CNV的发生会对人类健康影响更严重:与一直以来研究较多的单核苷酸多态性(SNPs)和病理性的单核苷酸变异相比,CNV发生的频率虽偏低,但累及的序列长度、基因数目、核苷酸数目却明显超过了前者,对基因组的影响比起SNP更大,一旦发生往往会给生命体带来重大缺陷,对人类健康和疾病的影响更为显著。将可能导致导致严重出生缺陷、癌症等。比如严重的脑病、心肌病、肌病、白血病、家族性遗传性结肠癌息肉病等等多种重大疾病,都和基因组的结构性变异直接相关。
3.
CNV是明确部分新的原发性疾病的重要手段:CNV具有很高形成速率,是多种新的未知疾病的发生原因。CNV的形成与众所周知的非同源末端连接,以及新近提出的DNA复制扰动和不连续DNA复制有关。多种机制共同作用,原发性CNV的形成速度远远超过其他类型的基因变异,导致一些新型疾病、疑难疾病、多系统交叉疾病的出现,CNV是明确这些疾病的重要手段。
4.
CNV是产前重大遗传病和家族性遗传疾病的预防诊断必不可少的:人类已知的染色体疾病有数百种之多。大片段CNV异常,统称为染色体微缺失/微重复综合征,这种大片段的DNA缺失或者重复是严重染色体疾病的主要原因,全基因CNV检测对产前诊断和产后家族性基因异常的评估,优生优育等具有重要意义。
5.
CNV是多学科多种疾病发生的重要原因:不仅严重的染色体异常如微缺失/微重复综合征与CNV密切相关,同时大量小片段的CNV或者累及单基因的CNV也是很多疾病的致病原因。CNV可存在于所有23对染色体中的任一或者多个、在全基因组的任何区域均可发生,可能涉及单个基因或者多个基因,可累及致病基因或者非致病基因,也可以是小片段或者大片段或者累及整个染色体长臂或者短臂,因此,CNV的类型多种多样,千变万化,导致疾病的多样化。
不同区域的CNV可造成不同的机体功能异常,致病性的CNV可导致人体器官先天异常(例如先天畸形、肢体残疾、发育迟缓、智力障碍)、多种关键酶学缺陷、多种神经系统疾病(例如PWAS综合征,多种肌病)、心血管系统疾病(例如肥厚性心肌病、致命性的长QT综合征)、免疫系统疾病(例如免疫缺陷综合征)、线粒体系统(例如眼外肌萎缩等等)、以及多种肿瘤(HNPCC遗传性结肠癌、胰腺癌)等数百种疾病发生等等。各个医学学科中大量的遗传疾病、诊断不明的疾病可能由于CNV的存在而造成,急需要从基因水平提供明确的诊断依据和为治疗方案的选择提供参考。
全基因组WGS分析替代一般基因检测的必要性
我国是一个人口大国,2018全年出生人口1523万,在出生缺陷发生率高达5.6%的情况下,每年新增出生缺陷人口巨大,给国家、社会和家庭带来了严重的负担,其中染色体畸变约占出生缺陷遗传学病因的80%以上,具体包含染色体数目异常、大片段缺失/重复及致病性基因组拷贝数变异(pCNVs)等。
染色体核型技术一直被认为是诊断染色体畸变的“金标准”,但由于其检测周期长、分辨率低、无法检出5Mb以下的CNVs等因素,使核型的应用受到了限制。之后从国外引进染色体微阵列分析(chromosomal
microarray analysis,CMA),然而由于该技术成本高、通量低且所使用的芯片探针覆盖范围有限,不能精确定位、可能导致部分小的病理性的CNV无法被检出等,限制了其在遗传疾病中的大规模应用。
基于下一代测序(NGS)技术的基因组拷贝数变异测序(WGS)和全为产前诊断和遗传疾病诊断提供了新的手段。WGS采用对样本DNA进行低深度全基因组测序,将测序结果与人类参考基因组碱基序列进行比对,通过生物信息分析以发现受检样本存在的CNVs。与核型分析、染色体微阵列分析等其他技术相比,WGS技术具有检测范围广、通量高、操作简便、兼容性好、所需DNA样本量低等优点。对于WGS技术检测结果的准确性,已在美国等西方国家经过部分临床样本的实际检测。
研究表明CNV偏向分布于基因超保守区域外的位置,多达40%的CNV位于基因沙漠区(gene
deserts)。但大部分的CNV涉及编码基因,一般的检测方法都存在很多的局限性和不足,例如MLPA方法只能检测单基因小片段的CNV,基因芯片技术无法精确判断断点位置,外显子测序集中在外显子区域,不能测定断点位于内含子和基因间区的CNV。事实上大量的CNV断点位于基因间隔区或者位于基因内含子非编码区,这些方法都会导致大量的CNV遗漏和无法检出。目前只有全基因组测序能够全面检测基因组中的CNV并精确CNV断点。研究发现平均低覆盖度WGS相较基因芯片CMA能检测出多于5倍的CNV,WGS的敏感性明显优于基因芯片CMA。
CNV全基因组关联分析对于传统的基于单核苷酸多态性的关联分析具有互补性,通过同时认识基因组结构变异可以认识复杂疾病的分子机制和遗传基础。目前国内基因组拷贝数目变异CNV临床应用的严重不足,是因为检测和诊断水准尚待提升,而开发基因组拷贝数目变异(CNV)临床检测应用的意义则是挖掘和发展其具有更新更广更精更深的诊断优势所长。随着中国相关诊断供给能力的提升,大规模相关诊断临床实践经验和中国CNV大数据的积累必定会大大推动中国相关临床学科诊断依据和治疗方案能力的提升。
国际国内CNV应用局限性和主要存在的问题
1.
应用领域的片面性:目前在国内只有极为少数具有技术条件和资质的医疗机构和公司进行CNV的研究和临床应用,主要应用在儿童复杂罕见遗传病、自然流产新生儿死亡等妊娠常务的遗传学检测、产前诊断核型异常的进一步异常分析,应用范围局限,积累的经验少。事实上,CNV的存在是人类的很多疾病的原因,包括多种肿瘤(结肠癌、肺癌、胰腺癌、内分泌肿瘤、颅内肿瘤等)、罕见疾病、多种神经系统疾病、多种心血管疾病、多种代谢疾病,线粒体疾病的CNV检测在国内尚未有效开展,亟待开发并应用于临床多学科。
2.
检出率的低下:不同的CNV检测平台和基因芯片的分辨率会造成同一样本得出不同的检测结果。目前的国内采用的方法主要是低分辨的基因芯片,因此造成很多有意义的病理性的CNV不能检测,例如一般公司基因的检测精度在5KB大小的缺失和重复,事实上,在人类基因组不仅存在大片段的CNV,同样也存在大量的小片段CNV涉及到单个基因和单个基因的外显子,这些也是造成疾病的重要原因。由于技术和仪器精度的不够使得这个片段被大量错失不能检出。另外也有大量的病理性CNV起始点和终止点存在于基因内含子,常规方法都不能够检测到,从而造成大量的漏诊和误诊。目前国内仅有极少数公司开展CNV相关的检测,但都存在低精度的问题。
3.
检测结果的验证缺乏规范化。新技术的发展、成熟和应用,必然会对临床体系产生巨大影响。目前在国内临床CNV诊断的实践中,各级医务人员没有统一的认识来如何正确定适宜的临床适应症,对CNV技术的临床使用中的技术路线、遗传咨询、应用规范、差异性结果的判定以及临床研究方向,都是亟待解决的重大课题。
4.
检测结果判读能力缺乏:对CNV判读能力的不足时困扰分析人员的最大问题,也是造成在国内CNV应用受到限制的主要原因,如果不能正确和全面的判读检测结果,将不能为临床提供有效和精确的诊断。对于罕见的新生CNV,嵌合体CNV、不同外显率CNV的判读和解释依然非常困难。后面部分将对本项目团队在这方面的优势和经验做进一步的阐述。
国际学术界解读CNV临床意义的难点
随着CMA、CNV-seq、WES、WGS等高分辨率技术应用于人类基因组CNV检测,临床上检测出大量的CNV片段。对于如何解读检测出的CNV临床意义,长期困扰着临床医生和基因检测机构。基因变异的解读作为遗传咨询工作中重要组成部分,也是最具有挑战性的工作,在我们基因变异的解读仍然是面临的重大问题。
1.
缺乏科学完善可靠的判读标准:国际学术界而言,CNV解读流程都是参考CNV与人群多态性数据库、微缺失/微重复综合征数据库、基因组异构数据库、网络数据库、文献中报道以及是否包含重要功能性基因等来确定临床意义。2015年美国遗传病协会ACMG发表一个初步简单的CNV临床意义分析指南,基因CNV变异的解读基本都是基于这个指南,但它是很不完善一种框架化的指导,但只是一个方向性的指导,可操作性弱,对于CNV重复和复杂的CNV的解读并不适应,无法满足特定的临床环境。
2.
判读结果的误差和不一致:近期的研究表明,即使使用相同的解读框架,不同实验室的病理学家也存在分歧,甚至在某些情况下,对于同一个变异的致病性,不同机构会有着截然不同的结论。在2016年美国分子病理学会(AMP)年会上,研究人员曾分享了来自于AMP工作小组名为“VITAL项目”的早期研究数据,该计划旨在揭示不同实验室对于相同遗传变异的解读存在差异的确切原因。结果显示,即使AMP采用使变异解读更统一的策略或依据指南,差异也仍然存在。
3.
人类CNV结构的复杂性与多样性:人类可能存在的CNV达数万种之多, CNV可存在于人类基因组中任何区域,大小尺寸、累及区域、受累基因、受累功能基团等都可能不同,形式多种多样,导致疾病的临床表现型千变万化。同时,不同的CNV也可能出现相同临床表现型,不仅已经检测到很多致病性的CNV存在,同时也存在大量非致病性的CNV。因此,区分致病与非致病CNV,正确评估CNV基因型与表现型的关联这些结果判读中的难点。
4.
个性特征、遗传方式的复杂性:由于CNV致病性的分析是非常复杂的过程,需要考虑许多证据、个性特征以及了解证据的复杂性,目前在制定完整而全面的评判标准非常困难,各基因诊断机构都缺乏正式和完整的判定标定。在一个缺乏标准化的领域中,难免会遇到定义模糊的问题,在评估指标、疾病关联等方面急需要细化和拓展。
5.
大量无效基因和多态性CNV的干扰。基因组结构中也存在大量假基因、非转录基因,这些无效基因会对CNV和正常编码基因的拷贝数目的判定与意义的评估带来强烈的干扰。大量的多态性CNV和非致病性CNV的存在导致部分新发现CNV不能够给出准确和正确的病理学分类,只能给与一个模糊和的不明确临床意义的结论。
由于上述种种因素的存在,CNV的解读是目前本领域最困难和最具挑战性的。本项目正是针对这种国际国内一直面临的困局开发一种前沿性的解决方案或建立一种新型评判量化标准。
项目组在CNV临床检测的技术实力和目标
目前美国三大临床检验公司(LabCorp,Quest,Bioreference),目前,只有Bioreference旗下的基因诊断公司从2019年初开始尝试采用WGS进行CNV检测,但也属于初始阶段。我们期待利用本项目的技术实力所长,奠定在CNV检测和评判方面的行业技术优势,并协助带动和提高中国基因CNV诊断水平到一个新的高度。
1.
优势高端技术人才:团队技术高管曾经作为教授、主任医师、研究生导师在中国顶级医疗机构解放军总医院进行临床、科研和教学多年,不仅具有在中国的丰富临床经验和医疗资质。同时作为首席技术科学家、项目经理、技术主管等在美国著名大学医学院、科研机构、基因诊断公司从事20多年的分子生物和遗传诊断研究、临床、科研和教学,在临床医学、遗传研究、基因诊断领域积累了丰富的经验。具备有足够分子诊断技术实力实施国际一流水准的全面而准确的基因诊断服务。
2.
采用世界最先进的高通量CNV检测设备:使用与美国类似项目的同步使用技术和设备,保持国内类似项目的领先实验室水准进行CNV检测。
3.
项目组已成功完成多个大型数据库的整合:可为CNV结果的判读提供可靠的依据和保障。
1) 健康人群CNV多态性数据库
2) 全基因组参考基因文库
3) 全基因组基因功能结构域数据库
4) 全基因组基因功能与疾病关联数据库
5) 全基因组大片段微缺失微重复综合征疾病数据库
6) CNV发生频率数据库
7) 临床CNV特征与意义数据库
8) 全基因组基因启动子与增强子定位数据库
9) 基因剂量不平衡预测数据库
10)
基因功能丧失耐受能力评估数据库
11)
蛋白编码与非编码基因类型数据库
12)
全基因组假基因与SegDup数据库
13)
发育迟缓CNV数据库
14)
基因回顾与基因交互数据库
15)
编码基因进化保留区数据库
16)
全基因GC含量数据库
17)
功能丧失与功能增强基因数据库
18)
单基因与微缺失、微重复遗传方式数据库
19)
全基因组微卫星与串联重复片段数据库
20)
开放阅读框架结构数据库与自动化判定
21)
全基因组基因外显子定位数据库
22)
PolyA定位数据库
23)
CYTO条带基因组定位数据库
24)
FISH探针数据库
4.
领先的CNV相关分析技术:本项目组团队掌握并独创了多种与基因突变分析相关的技术,希望在未来通过我们的努力将这些分析方法应用到CNV的临床意义的评定方面,并制定了一整套属于本项目独特和独有的CNV致病性的量化指标与评判标准,包括单基因疾病和多基因疾病的致病意义的标准,这将对提高诊断评判的一致性,对临床致病性分析具有重大的意义,而且可为临床提供准确而又具有诊断和指导意义的检验结果报告。
25)
拷贝数目变异定位与结构分析
26)
基因组变异数据库正常人群发生频率比对分析
27)
已知和相邻大片段微缺失微重复综合征数据库比对分析
28)
已知和相邻小片段缺失与重复的疾病数据库比对分析
29)
特定疾病的相关最小重复区域分析
30)
区域内基因受累结构与蛋白功能判定分析
31)
无效等位基因分析
32)
基因截断与延伸分析与判定
33)
开放阅读框架分析
34)
染色体倍性分析
35)
受累基因功能结构域分析
36)
功能基因分析,包括单基因疾病,多基因疾病的致病性关联分析
37)
遗传方式分析
38)
剂量不平衡分析
39)
重点结构区域进化保留区分析
40)
受累基因功能丧失与功能增强的分析
41)
突变耐受性分析
42)
串联重复结构分析
43)
杂合性丢失与单亲缘二倍体检测分析
44)
基因型与表达型的关联分析
45)
综合文献分析
5.创立CNV病理学意义评估知识体系成果:团队成员在美国Lombardi肿瘤中心分子与遗传研究所建立和发展线粒体基因诊断等多项分子技术、为美国纽约Downstate医学中心建立基因诊断临床实验中心,在美国最大基因检测诊断公司开展了美国及全球临床检测诊断业务,具有基因组拷贝数变异(CNV)检测与病理学意义评估诊断标准的大量经验及知识体系成果,在经验积累的基础上已经基本完成本项目独有的大尺度CNV和小片段CNV,多基因和单基因CNV的全面的、科学的、可操作的解读量化指标评估系统,形成了成熟可靠的可以直接引进产业体系应用于中国人群的疾病基因诊断,有效弥补国内在这方面的空白和缺陷。
基因诊断系统框架结构和量化指标评估分析系统:暂时省略
全基因组测序WGS进行CNV检测的主要优势
1.覆盖度全面:指基因组被测序得到的碱基覆盖的比例。WGS覆盖更多的基因,目前全外显子测序WES覆盖的基因为21000个左右,而WGS则覆盖目前已知的人类所有基因约25000个左右。WGS对具体每个基因的覆盖度更好,由于基因序列的特殊结构(如高GC含量或串联重复区)外显子测序在该区域探针设计存在困难,而WGS不存在这样的问题。
2.测序深度大:是指测序得到的碱基总量(bp)与基因组大小的比值,它是评价测序量的指标之一。测序深度与基因组覆盖度之间是一个正相关的关系,测序带来的错误率或假阳性结果会随着测序深度的提升而下降。WGS不仅可检测所有的外显子,而且可以检测内含子区,虽说人类疾病有80%在外显子区,那也有200%是在内含子区,主要的致病基因可能是影响了转录本的剪切。由于绝大多数的CNV的断点位置并不位于外显子,而是存在于内含子,目前,只有WGS和基因芯片技术能够有效检测到这些CNV。
3.线粒体基因组:WGS测序深度有2000-8000X,可以准确测定线粒体基因组变异。而外显子测序捕获区域一般不包括线粒体基因组,即使在IGV查看外显子bam文件,也会发现在线粒体中也会有一些少量的reads,但这些都不是特异的,不可信,需要联合一代测序检测线粒体基因组。
4.分辨率高:WGS可以检测大片段的插入缺少(CNV)而且结果非常准确、检出率高。而外显子测序基本不可以检测CNV,即使通过软件(如CODEX,XHMM)计算CNV也存在假阳性及假阴性太高的问题。目前科研及临床都是用基因芯片来检测CNV,但是WGS检测CNV的分辨率在碱基水平,而密度最高芯片分辨率也在10K以上,即使一些特殊设计在外显子上的芯片,由于芯片本身探针效应等问题也很难达到宣称的外显子分辨率。
5.断点位置精确:WGS技术不仅能够检测大片段区域性的重排,而且能检测小片段的的CNV,检测精度理论上可以实现检测到100bp甚至更小的CNV,精确的确定断点位置,因此可以检测到很多尚未报道的未知的基因突变和CNV。
6.复杂CNV检测优势:WGS还可以检测平衡移位,如倒位与易位等等复杂的CNV。
下图显示了常规检测与全基因组CNV检测的优缺点

正因为以上几点优势,WGS在临床致病基因检出率更高,如严重智力障碍WGS检出率为>60%左右,而全外显子测序为<30%左右,自闭症WGS检出率为>50%左右,全外显子为15-20%左右;简单来说,WGS检测CNV和核苷酸变异的能力大于全外+芯片+线粒体测序,是目前最全面检测基因变异和最具发展前景的疾病诊断方法
拟采用的主要技术与设备
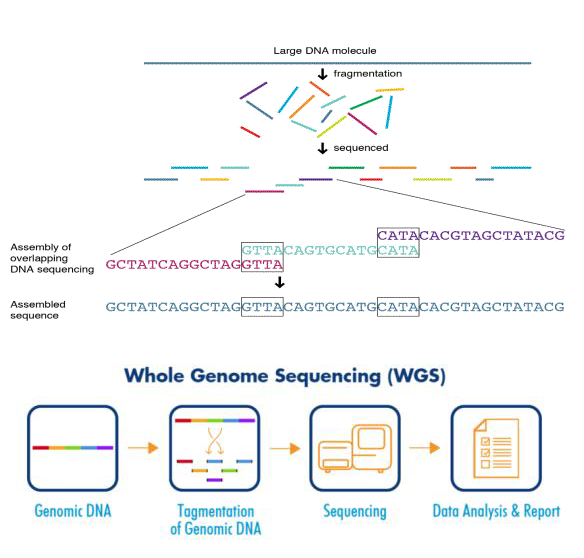
设备:NextSeq550Dx仪器:已获得批准供体外诊断使用。可应用与诊断模式:NGSIVD应用。研究模式:全基因组测序和全外显子组测序,靶向基因测序(扩增子、基因panel),全转录组测序,细胞遗传学芯片。双重测序模式可用于临床检测和各种临床研究应用
试剂:NextSeq500/550v2试剂盒

2.
辅助检测与结果验证设备:Agilent或者Affymnetrix全基因组比较芯片技术。
Affymetrix和Agilent aCGH/CNV芯片的探针覆盖所有基因组,在包括基因区域(内含子区、外显子区)、基因间区域以及对疾病研究极其重要的亚端粒区域(除重复序列外)的分布大致相同。因此,利用此平台进行CGH分析具有敏感度高、精确度高,分辨率高(平均分辨率1.4kb)的特点,同时还可检测福尔马林固定的石蜡样品,实验数据可信度高,仅需1.5μg基因组DNA即可进行实验。
设备:SureScanDx微阵列芯片扫描仪:Agilent
SureScanDx微阵列芯片扫描仪已通过CE认证,可在美国以外的许多国家/地区用于体外诊断(IVD)。SureScanDx微阵列芯片扫描仪在美国为II级,510(k)豁免。该高灵敏度系统体积小巧,在提高灵敏度并保持最宽动态范围(XDR)的同时可为实验室节省更多空间。作为完整微阵列芯片解决方案的基础,SureScanDx微阵列芯片扫描仪系统可以灵活地分析许多基因组学和细胞遗传学微阵列芯片。该系统还具有内置的臭氧防护系统,可最大限度减少信号衰减,此外还具有连续芯片加载功能,可加快使用速度。
试剂:CGH+SNP微阵列芯片


3.
DNA自动化抽提设备(50000RMB)
ThermoFisher
KingFisherFlex:高通量自动化DNA提取

4.
实时定量PCR系统:ThermoFisher
QuantStudio™7Pro Real-Time PCRSystem

5.
扩增工作台AirClean600

6.基因分析仪
Applied
Biosystems SeqStudio Genetic Analyzer

7. 其它:计算机服务器系统、离心机、加样设备等。
基因组拷贝数目变异(CNV)临床检测项目市场行业定位
基因测序行业的上游为测序仪、测序试剂和耗材的供应商,代表公司为Illumina、ThermoFisher、Roche等;中游主要是测序服务机构以及生物信息分析机构,代表公司为华大基因、贝瑞基因、达安基因、迪安诊断、Illumina等;下游为测序服务的用户,主要是个人、医院、制药企业、政府研究机构、高校研究机构等。
测序技术的演化和进步是测序市场发生发展的原动力。当前第三代测序成熟和大规模应用仍需时日,未来很长时间内二代测序仍将是测序市场的中流砥柱。对测序平台性能和价值的衡量应当紧密围绕读长、通量、准确度和成本四个因素进行考量。在进行不同目的的基因检测时,对测序深度和的覆盖度的权衡是成功测序策略的关键。测序上游产品技术壁垒极高,国际市场基本被Illumina和ThermoFisher瓜分,对国内下游服务企业造成较大成本压力。国内企业拥有自主测序平台能有效提升企业整体竞争力,但应仔细考察其技术来源和性能指标。
我们重点看好国内企业在中游和下游测序服务市场有所作为。不同细分领域方面:研究服务市场目前相对饱和,竞争激烈,未来技术进步有望创造行业重新集中的契机;生育健康市场目前已有一些产品,是当前基因测序产业收入规模最大的细分市场,未来仍将大机率保持稳健快速成长,相关公司也已在登陆A股市场进程中;肿瘤基因测序特别是早期肿瘤筛查──液体活检领域是基因测序领域下一个最有希望的「杀手级应用」和投资重点,其潜在市场空间远大于生育健康类服务,但技术难度大,目前仍在成熟成长,由科研向临床转化阶段,企业的技术能力和渠道能力十分关键;消费级测序领域产品化空间广阔,但目前规范化程度低,鱼龙混杂,销售能力是最重要制胜法宝。
开发基因组拷贝数目变异(CNV)临床检测应用的项目属于基因测序行业的中游。拷贝数变异(CNV)在人类基因组中广泛分布,极大地丰富了基因组遗传变异的多样性。目前已经发现大量的基因病是由基因组结构改变引起的,而非传统的碱基配对变化所引起,其中一些基因病是由重组区域的基因拷贝数发生改变所致。研究发现,大部分拷贝数变异(CNV)都与复杂疾病密切相关,其检测将会在未来广泛应用到临床各个学科,不仅产前、而却在神经、心血管、肿瘤、风湿、消化、免疫、血液系统等等多疾病的诊断中。
解读或分析基因数据的评判标准,以体现基因测序的意义,这才是一项最实际的应用,这属于基因测序行的中游服务链的最重要的一个环节,或关键点。本项目的目标之一就是打通这个环节,拓展新一代的人类疾病基因组诊断服务产业。
随着中国相关诊断供给能力的提升,大规模相关诊断临床实践经验和中国CNV大数据的积累必定会大大推动中国相关临床学科诊断依据和治疗方案能力的提升。
基因组拷贝数目变异(CNV)临床检测项目市场现状
当前人们对拷贝数变异与疾病关系的认识主要集中于发育疾病、感染与免疫疾病、神经系统疾病以及各类肿瘤。
国内对拷贝数变异与疾病关系的认识主要集中于产前遗传疾病,发育疾病。目前,在全国十大基因公司中,开展CNV检测业务的有三家,即:贝瑞和康,安诺优达,华大基因,且以贝瑞和康的贝全安-WES+CNV-Seq服务套餐较为领先。三家公司的业务局限于产前诊断。
在相关检测技术快速发展的推动下,人们已经发现了诸多与各类疾病发生密切相关的拷贝数变异。美国等世界一流的机构已经开展研究探索CNV与感染、免疫疾病、心血管疾病、内分泌疾病、神经系统疾病以及各类肿瘤的关系,并开始逐步应用于临床诊断和家族高风险人群的评估。
2018年3月份,美国基因检测公司23andMe获得了FDA(美国食品药品监督管理局)的批准,可以在没有医生处方的情况下,向消费者提供特定的癌症基因检测产品。这意味着美国基因检测行业监管进一步放宽。同一天,立足消费级基因检测的国内公司23魔方宣布完成新一轮融资,总额1亿元人民币。前瞻产业研究院预计,未来五年我国基因检测复合增速在35%左右,2020年有望突破300亿,更长远的潜在市场过千亿。
本项目拟开展的业务在目前市场上的优势
1.本项目组拟采用世界最先进的高通量CNV检测设备:使用与美国类似项目的同步使用技术和设备,保持国内类似项目的领先实验室水准进行CNV检测。
2.本项目组已成功完成多个大型数据库的整合:可为CNV结果的判读提供可靠的依据和保障。
3.本项目选择对CNV检测有成本效果的技术基础上,建立一个CNV诊断评估标准,开发一个精确的分析工具,降低CNV诊断评估成本,能更广泛开拓市场。
因此,本项目组将在国内开拓基因组学的具有国际最前沿水准的CNV人类疾病的诊断分析业务,其中,包括国内一些大型基因公司已经开展的业务;但会比国内目前的已经开展的业务更全面,也会更精确,更会具有成本效益的竞争优势。
基因组拷贝数目变异(CNV)相关法律与监管方面
国家卫生计生委的职责是审查和规范基因检测机构的资质,国家食药监总局则对基因检测链上的仪器、试剂、分析软件进行监管。
基因检测涉及的伦理、隐私、遗传信息保护和生物安全等问题尚未得到明确和统一的监管。
如果从事疾病检测或者产前检测,卫计委、国家食药监总局等会要求一些许可和相应的证书。
国内已经有基因组拷贝数目变异(CNV)产前诊断的临床检测的应用,说明监管方面“支持、鼓励前沿技术和产品在通过安全性、有效性评价的基础上尽早惠及公众”。
第二部分 项目实施
国际上,目前本项目组高层次人才在基因组拷贝数变异(copy number
variations,CNVs)的人类疾病诊断分析的知识体系和经验都是处于最前沿,也已经在美国开展了理论与实际结合的应用;进一步对这种知识体系与经验相结合的成果进行总结发表,在短时间内就可以成为一个满足人民健康需要的应用型新产品--CNV标准化疾病诊断分析工具;而且,通过这种新型诊断工具的实际应用,也可以使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。借助这种趋势,也有望通过科学研究和科学管理相结合的方式把本项目的实验室建设成具有国家重点实验室性质的CNV国际研究中心之一。
为实现这些目标,项目组希望通过海外高层次人才以“项目+团队”的方式落户国内,期望得到当地政府的支持和帮助,期望在具有开放和创新之地的城市中,将本项目富有成效地开展起来。
项目目标
依托创新的检测技术、精准的检测方法和严谨的科学态度,实现:
1.
建立国际一流水准的全基因组CNV诊断分析实验室。
(国家重点实验室性质)
2. 建立国际前沿水准的全基因组CNV诊断分析标准。
3. 转化和实施全基因组CNV诊断分析标准的市场化。
4.增加科研开发能力,带动和提高中国基因诊断水平到一个新的高度。
项目策略
1.组建公司:
实验室独立经营模式即基因检测公司独立组建实验检测中心。
项目初期建立主要采用基于采用与美国类似项目的同步使用技术和设备,保持国内类似项目的领先实验室水准进行CNV检测。项目选择对CNV检测有成本效果的技术基础上,建立一个CNV诊断评估标准,开发一个精确的分析工具。加入定量生物学和统计学方法,使得能够优化信噪比,从而降低CNV诊断评估成本。也使得CNV能更广泛开拓市场。利用与美国类似项目的的临床检测实验室和新型基因组拷贝数目变异(CNV)临床检测标准及诊断的高端人才优势,对国内尚未开展或开发的基因组拷贝数目变异(CNV)临床和非临床应用开展新的业务服务。
2.通过海外基因组拷贝数目变异(CNV)临床检测应用的高端专业人才的知识和技术,开发全基因组CNV诊断分析与病理学意义的评判标准。开发多基因和单基因的解读量化指标新标准。并推进二套标准的知识产权体系化和向市场化的转变。
3.在检测项目获得CFDA获得批准临床应用之前,与面向高端人群的医疗健康咨询体检机构和体检中心合作,加入CNV和相关的基因检测项目,实现实验中心建设完善期间,获得部分收入以补偿或支撑实验中心的日常运作。
4.进一步发展国际上的最新WGS技术的临床检测实验室。新WGS技术实验室不仅仅符合中国标准(参照《临床分子病理诊断实验室二代基因检测专家共识》),还将具备国际一流水准。对国内尚未开展或开发的临床和非临床应用进行新的业务。
5.建设本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。也有望通过科学研究和科学管理相结合的方式把本项目的实验室建设成具有国家重点实验室性质的CNV国际研究中心之一。
核心团队
本项目的核心团队成员包括四方面的人才层次:一是具有国际前沿水准的全基因CNV诊断分析领域的教授级专家;二是具有大型健康项目管理和国际大型金融机构工作经验的项目管理型专家;三是具有涉及基因领域的临床分子遗传疾病和疑难杂病医学专家,提供直接的临床医学指导;四是具有国内企业上市、并购重组、财务顾问等业务的实际操作经验的经济学专家。
在核心团队成员的基础上,将通过吸收、招聘和培训等方式,建立起项目执行团队,完成项目的开展与实施。
毕业于中南大学湘雅医学院医疗系和解放军总医院军医进修学院;研究生导师;从事临床医学、遗传学与肿瘤研究三十多年;先后参与中国国家基础研究规划项目课题研究,美国国防部和国立卫生研究院自主的多项课题研究。先后在美国乔治城大学、纽约州立大学Downstate医学中心、美国三大基因检验公司中的QUEST和BIOREFERENCE从事人类疾病基因学研究和诊断工作近二十年;在美国BIOREFERENCE公司担任基因组拷贝数目变异(CNV)项目首席科学家及该项目研究团队负责人五年;率先开展了该CNV项目的全球(主要是殴美发达国家)最具学术前沿的诊断业务,多项学术成果发表在美国遗传学杂志、肿瘤研究等国际学术期刊上,拥有非常丰富的人类疾病基因学的知识和经验。
公共健康硕士 项目创始人 医学健康和金融领域项目管理专家
毕业于中南大学湘雅医学院医疗系和美国EMORY大学;先后从事国家卫生部、世界卫生组织(WHO)、世界银行(WORLD BANK)、美国疾病控制中心(CDC)大型健康项目研究和管理工作十多年;在国际大型金融集团的美国大都会保险公司(METLIFE)、加拿大明信理财集团(CLARICA)和永明金融集团(SUNLIFE)工作二十年;拥有丰富的项目市场开发工作经验和项目管理、基金、保险、税务、投资等专业(具相关行业或专业资质证书)工作经验。熟悉大型管理机构工作程序和大型企业的企业文化。主要获奖:联合国开发计划署项目管理研究成果奖;美国大都会保险公司成就奖。
临床医学博士 教授 项目创始人 临床分子遗传疾病医学专家
毕业于中南大学湘雅医学院医疗系和解放军总医院军医进修学院;主任医师;临床医学研究生导师;教授;从事临床医学三十多年;先后在中南大学湘雅医学院附二医院、中国人民解放军总医学、老年心血管病研究所和救治中心、美国乔治城大学医学中心、新泽西医学中心、美国首都华盛顿医学中心等世界著名医疗机构从事内科疑难疾病、分子遗传疾病、心血管疾病临床工作、科研、教学;具有丰富的临床疑难疾病、分子遗传疾病的诊断经验,并进行了多项相关课题的研究,多项研究成果发表在一流的生物医学杂志。
高级经济师 项目合伙人 企业财务管理专家
毕业于湖南财经学院;1993年开始从事投资银行工作;先后任职于北京京华信托、大鹏证券、国元证券、湘财证券、中山证券、五矿证券等单位;全国首届经济师获得者,通过首届证券投行从业资格考试;主持山东浪潮、山东电缆、鲁银投资、正虹科技、银山化工等公司IPO上市业务;对企业上市、并购重组、财务顾问等业务具有丰富的实际操作经验。
项目协作单位/医学领域医疗顾问名单:
。。。。。
(注:医学专家群汇集了全国各学科专家和优秀医疗资源。基于项目需要,本项目还有更多的医学领域资源可以请各个医学领域的专家教授给予指导。)
拟开展的CNV和基因变异检测项目
CNV变异涉及到几乎所有的临床学科,数百上千种疾病涉及CNV的异常,包括遗传病、心血管疾病、肿瘤、神经疾病、结缔组织疾病等等。CNV的检测可为这些疾病的从基因水平提供诊断依据和治疗方案的选择提供参考意见。
本项目拟开展和逐步开展的CNV和基因变异检测主要内容或清单列在附件(拟开展的CNV和基因变异检测项目)之中,这些内容是目前比较前沿的临床检测,可以成为本项目的特色基因检验服务套餐或其它方式而开拓新的市场。
实施计划
第一年
1.组建公司
实验室独立经营模式即基因检测公司独立组建实验检测中心。
公司组织机构包括三个部分,即:决策机构(董事会)、执行机构(总经理及部门经理)和监督机构(项目投资方及相关监管方)。
为有效进行项目的建立和运作,公司初期的组织架构关系如下:
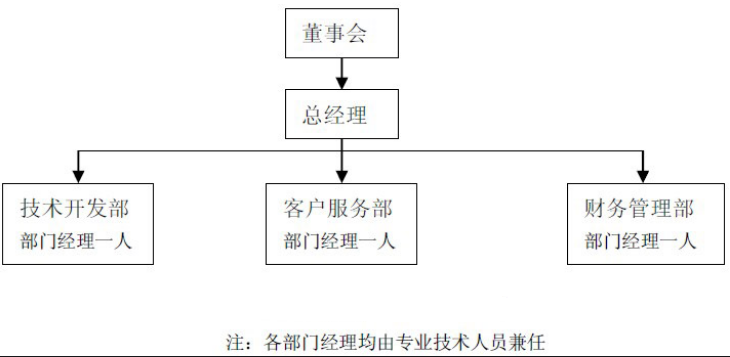
(注:将通过吸收、招聘和培训等方式,建立起项目执行团队,完成项目的开展与实施。)
2.建立与美国类似项目的同步使用技术和设备的国际一流水准临床检测实验室及诊断评判新标准。
仪器设备和试剂: 美国公司产品为主。并根据需要配置其它相关实验,办公,等仪器和设施。
3.增添能开展其它基因检测业务的设备及人员;布局全面的基因检测市场。
第二年
1.开展国内尚未开展的基因组拷贝数目变异(CNV)临床和非临床应用的新型业务。
2.在第二年底前,培训致少二位具有高端水准的出具检测诊断报告人员,实验技术操作人员4-6人。
3.在第二年底前,增添设备,扩大服务规模;开发全面的基因检测市场。开拓各种可行的市场营销模式。
建成实验室标准
|
检测和诊断水准: |
达到基因组拷贝数目变异(CNV)的国际前沿 |
|
|
国内开创性的领先水准 |
|
|
|
|
诊断评估报告: |
达到平均每天发送60份(CNV)的潜在能力 |
|
|
(大约年总量为20000万份的的潜在能力) |
第三年及其以后
1.监管项目开展,建立和扩大业务市场,增加赢利。
2.进一步发展国际上的最新WGS技术的临床检测实验室。
3.项目执行顺利的情况下,考虑项目更长远的规划,包括科研开发和企业上市等等事项的布局。
初期市场和营销
基因组拷贝数目变异(CNV)临床检测的目标客户
客户包括:
个人、医院、制药企业、政府研究机构、高校研究机构,也包括健康人群、高危人群,也可辅助治疗、预后监控。基因组拷贝数目变异(CNV)可应用于临床和非临床方面,临床上,基因测序可用在生育健康检测、病原体感染检测和肿瘤基因检测。非临床上,可用于基础医学研究、新药研发、农牧业育种、生物多样性保护、司法鉴定、环境污染治理等。
客户渠道:
主要的客户渠道是中大型医院临床检测:涉及临床学科的方方面面,绝大部分医院不能自行开展这些检测。本项目组团队成员和协作顾问中,几乎都有医学背景,非常熟悉行业情况,具有非常强大的临床医学检验市场的开拓能力。
其它可以根据市场情况的变化进行适应调整,例如:
健康管理的综合类检测:让消费者对自己的基因遗传情况以及患病可能有一定了解。
直接面向顾客(direct to consumer, DTC) 类检测:了解家族历史、遗传疾病潜在风险,更好地规划生活、规范行为。
市场营销模式
1.在实验室独立经营模式基础上,通过与医疗机构合作经营模式,与医疗机构外包合作模式,以及共建联合实验室等多种方式进行市场开发。
2.在越来越多的各种委托第三方医学检验机构的招标项目中,积极参与各种委托第三方医学检验机构的投标项目。
3.根据需要,选择直接面向顾客(DTC)模式,指在没有医疗人员参与的情况下,直接向消费者销售的体外诊断产品模式。消费级DTC基因检测产品的消费全流程一般包括五步:购买检测、绑定账号、唾液采样、回寄试管、查看报告
4.传统广告,文宣,社会公益活动等多种形式提升企业知名度和企业形像。
主要业务方面
利用本项目的特点,进行有针对性的市场推广,力求把下面几个方面的检测、解读做精、做细,从而形成差异化竞争:
单基因疾病和多基因疾病的基因检测
肿瘤风险的筛查
生育健康
遗传病诊断
复杂疾病诊断
心血管遗传病诊断
代谢疾病
神经系统疾病
线粒体疾病
其它潜在市场
例如,寻找参与遗传性肿瘤综合干预业务的诊断分析市场与机会
成本效益
本项目符合中国精准医疗服务、《“十三五”生物技术创新专项规划》和《国家生物技术发展战略纲要》编制的政策提倡,是国家在这些整体战略目标和政策的社会效益方面的一个具体落实和体现之处。
基因检测属于高投入高利润的检测项目,也是未来明确疾病诊断的黄金标准。如果能够获得审批,开展临床服务,会带来巨大的经济和社会效益。
美国三大临床检验公司(AmerCorp, Quest, Bioreference)之一的Bioreference旗下的geneDx从2019年初开始尝试采用WGS进行CNV检测,代表着一个新兴的生物学应用行业的兴起。
本项目将基于保持和国际前沿水准相近的目标,以小而精的设备和人员规模来控制成本的策略,实施边建设实验室边开展可能有的业务方式,实现建成一个具有国际前沿水准的新一代基因组检测诊断实验室。有望通过科学研究和科学管理相结合的方式把本项目的实验室建设成具有国家重点实验室性质的CNV国际研究中心之一。
以本项目总投资3500万人民币的成本为考量,其直接效益--建成最新WGS技术的国际一流水准临床检测实验室(符合国家标准)--将是一个2000万级以上的开展服务和业务的实体平台;按本项目将带动国内一个新兴的生物学应用行业预测,必将是上亿规模的产业。
以本项在短时间内可以建成一个满足人民健康需要的应用型新产品--CNV标准化疾病诊断分析工具--在中国率先建立的具有知识产权性质的相应诊断评判新标准所带来的经济和社会效益,则是难以估量的,将把中国的基因组拷贝数变异(CNV)诊断水准提升到国际水准上,也或成为具有国际学术前沿水准的一个中国品牌,将更多更好地服务于人群健康的需要。
盈利计划
以本项的应用型新产品--CNV标准化疾病诊断分析工具--可以使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。这个诊断工具是本项目有知识产权性质和强大竞争力的核心产品。
项目建设周期预期为二年,第三年预期盈利,第四年预期回收投资总额,第五年预期纯盈利达4000--6000万水平的规模。
盈利估测 (全基因检验诊断分析)
|
|
保守性预估 |
平均性预估 |
实验室设计量 |
|
检验样本数(例/天) |
20 |
40 |
60 |
|
检验样本单价(元/例) |
10,000 |
10,000 |
10,000 |
|
全年有效开放天数 |
360 |
360 |
360 |
|
总营业收入 |
72,000,000 |
144,000,000 |
216,000,000 |
|
营业回报率 |
30% |
30% |
30% |
|
纯盈利收入 |
21,600,000 |
43,200,000 |
64,800,000 |
实验室开始运转的保守性预估:总营业收入在7千万左右规模,纯盈利收入在2千万左右规模。
实验室中期运转的平均性预估:总营业收入在1.4亿左右规模,纯盈利收入在4千万左右规模。
实验室设计量的平均性预估:总营业收入在2.1亿左右规模,纯盈利收入在6千万左右规模。
保守估计:
以保守平均每天20个检测样本,每个样本10000元人民币预计(注:基于美国已经开展的项目按国内情况估算),一年的产业规模就可达到7000万以上,其中,纯利润以30%计可达2100万。保守的每天20例样本预估是基于下列二种方式的市场必需可能性评估:
1.检测样本中,如果按病症来源可以估计如下:
肿瘤早筛:10-15例/每天(全年3650-5475例)
生育健康:6-8例/每天(全年2190-2920例)
少见病症:2-3例/每天(全年730--1095例)
复杂病症:2-4例/每天(全年730--1460例)
2.检测样本中,如果按送检来源可以估计如下:
来自全国医疗机构(约2万家):10-20例/每天(全年3650-7300例)
直接面向顾客方式(大众人群):10-20例/每天(全年3650-7300例)
3. 纯利润以30%计是基于下列考量:
2016年,华大公司实现营业收入17.1亿元,净利润5.87亿元,33.9%净利润率。(含非归属口利润2.37亿元)
2016年,贝瑞和康公司实现营业收入9.2亿元,净利润2.9亿元,31.5%净利润率。(含非归属口利润1.4亿元。)
具体计划:
第一年:组建公司并建立国际一流水准临床检测实验室及诊断评判新标准。
第二年:开展国内尚未开展的基因组拷贝数目变异(CNV)临床和非临床应用的新型业务。
第三年:建立和扩大业务市场,纯盈利预期不低于2000万元人民币。(以保守的平均每天20例样本的检测诊断计)
第四年:扩大市场,纯盈利预期不低于3000万人民币。(以平均每天30例样本的检测诊断计)
第五年:扩大市场,纯盈利预期不低于4000万人民币。(以保守的平均每天40例样本的检测诊断计)
其后:建立实验室其它分中心,期望下一个5年计划中保持20%的纯盈利收入增长速度。考虑项目更长远的规划,包括科研开发、更多服务项目开发和企业上市等等事项的布局。

具体计划中的考量是基于下列国内市场和行业参考数据:
国内三大上市医学独立实验室2018年营业情况:
|
企业名称 |
净利润(万元) |
同比上长 |
|
迪安诊断 |
32,963 |
49.53% |
|
金域医学 |
19,053 |
34.60% |
|
达安基因 |
10,158 |
17.51% |
(国内三大上市医学独立实验室2018的净利润都过亿,并且同比上长平均在30%以上。)
实际可能:
基因组拷贝数变异(CNV)诊断水准提升到国际水准上是医学临床和非临床的生物基因诊断未来发展方向和趋势所在,很大程度可以更充分开发其应用市场,并达到可观的盈利(实际达到产业规模上亿的可能性很大)。
1.随着中国中产阶层和富裕人群数量的增长,人们对自身健康和健康生活质量的重视程度也将相应更多的关注,而更新更广更精确的疾病筛查的诊断技术和能力也将在这些方面显示其市场需要性,而本项目的新型基因检测和诊断方法则是满足这种市场需要的时机点,相应的市场需求会越来越大。
2.肿瘤基因测序特别是早期肿瘤筛查──液体活检领域是基因测序领域下一个最有希望的「杀手级应用」和投资重点,其潜在市场空间远大于生育健康类服务。
3.一方面,基于精准医疗和现代健康管理模式,具体市场开发计划将会是多种形式;另一方面,基于人工智能和大数据时代,将导致或带来新的市场机遇。
4.开阔国际视野和市场,提前布局,国际多方多平台合作共赢市场模式也将是未来趋势。
资金需求
第一期(第一年) 融资需求
2000 万元人民币,主要用于:
1.组建公司、办公场地及设施:
120 万。
2.建立与美国类似项目同步使用技术和设备的临床检测实验室:1500
万。
3.人员:280
万。
第一年公司员工预设为8人,其中: 技术高管(1人);项目高管(1人);财经高管(1人);专业医生(1人);技术人员(2人);办公人员(2人)。
4.其它:100
万。

第二期(第二年) 融资需求
1500 万元人民币,主要用于:
1.市场开发:
600万。 (第一年节余部分可以考虑投入到市场开发中去)
2.办公场地及实验室维持业务运转的费用:
400 万。
3.人员:450
万。
第二年公司员工预设为16人,其中:技术高管(1人);项目高管(1人);财经高管(1人);专业医生(2人);技术人员(4人);办公人员(3人);市场营销(4人) 。
4.其它:50
万。
(注:因为市场的开发及增添能开展其它基因检测业务的设备及人员。项目也有可能开始部分创收。)

第三年及其以后:
实现盈利预期(盈利计划)
股份和股权
股份比例关系(细节待添加):
主要技术人员:股份 30%。
主要运作人员:股份 25%。
资金投资方面:股份 45%
(可按投资份额再另行分配比例)。
风险评估
投资风险主要体现在下面几个环节:
1.政策上的风险:主要包括国家对人类基因学研究与应用的限制性变化。例如,
1)相关资质的申请和获得政府批准:包括营业执照,检验许可证,检测中心实验室建设需符合国家标准。
2)检验许可所需的前期临床试验报告,需要获得CFDA审批。
3)前期试验和CFDA审批过程时间长,需要一年甚至更长时间。
2.市场上的风险:主要可能是如何开发市场的方面,需要让临床医务人员认识到新知识体系和新技术体系相结合的新型诊断标准工具如何能更好地服务于临床上,才能竞争更多的市场。
3.技术上的风险:生物技术发展相当快,这是今后我们的项目可能面临被超赶的风险。
风险控制
1.政策上:国际和国内的基因行业的法规和政策是趋于越来越开放,要把握好这种趋势来开拓相应的市场;本项目组项目管理团队深刻认识到这些,也清楚明白相关管理部门的管理方式,尽早避免这类风险。
2.市场上:在市场开拓上,多作调查研究,了解市场可能的真正难点和解决之道,及时调整市场开发策略,选择成本效果的方式进行市场开发和竞争。
3.技术上:在保持本项目已有的优势情况下,注重未来新的发展,及时更新知识和技术体系;注重吸收新的人才和更新必要的仪器设备;创建科研形式的实验研究项目,鼓励创新和专利发明。
4.其它:
1)做好前期融资工作。注重寻求当地政府的政策和财政支持。注重融资方面的潜在投资人或单位。
2)严格按国家标准建设实验室和安排有专业资格的岗位人员。
3)充分发挥和利用专业团队已有专业技术方面的知识和能力。一个项目的成功,主要取决于技术和管理二方面,项目组将着重于这二方面,以建成国际前沿水准的实验室而努力。
总体而言,只要建成最新WGS技术的国际一流水准临床检测实验室并可以开展业务,就达到了预期的初步目的,这种新的前沿性的下一代实验室服务实体的形成,具有市场竞争优势,可以进一步融资和/或开展其它合作机会。
以本项在短时间内可以建成一个满足人民健康需要的应用型新产品--CNV标准化疾病诊断分析工具--就可以使本项目的实验室成为全国第一个最前沿最全面的CNV疾病诊断分析中心。从成本效益的角度,国际一流水准临床检测实验室的建成也就足够可以补偿前期的资金总投入。
第三部分 附件
1. 市场和客户相关报告
市场相关报告
刚需产品调研及非刚需产品调研
2. 拟开展的CNV和基因变异检测项目
3. 项目核心团队人员简历
4. 深圳政府有关促进企业发展的政策支持
参考:我们关注的基因测序领域重点公司
1.市场和客户相关报告
市场相关报告
自2000年人类基因体计画完成以来,越来越多的基因功能被解读成功,已超过2000种基因相关疾病被发现,如今已有700多种基因相关疾病已开发出相应药物及治疗方法。含癌症与许多罕见疾病,其药物的开发与应用都正在进行。目前基因检测的技术已渐成熟,所检测出的基因型除了应用在诊断与治疗之外,甚至能依据资料库的内容经数位化统计方式,预测尚未发生疾病的风险。
2018年3月份,美国基因检测公司23andMe获得了FDA(美国食品药品监督管理局)的批准,可以在没有医生处方的情况下,向消费者提供特定的癌症基因检测产品。这意味着美国基因检测行业监管进一步放宽。同一天,立足消费级基因检测的国内公司23魔方宣布完成新一轮融资,总额1亿元人民币。前瞻产业研究院预计,未来五年我国基因检测复合增速在35%左右,2020年有望突破300亿,更长远的潜在市场过千亿。
现今基因检测主要的应用方向包含:
身分鉴识/亲子关系鉴定/追溯祖源
单基因/染色体遗传疾病诊断与带因筛检
临床预防医学:多基因遗传疾病基因检测
临床个体化医疗:药物基因体学
先天体质/特质潜能分析
基因检测相关企业主要有四类,一是采用“第三方医检所+医院+保险公司”的推广模式,针对临床基因、分子检测等项目,解决医疗机构医疗资源不足的问题,为民生相关的医疗服务奠定基础。二是通过引进及自主研发先进分子检测技术,提供分子诊断、基因检测、遗传性疾病及肿瘤早期筛查等服务,把基因检测的高端市场平民大众化,帮助受检者早诊早治。三是充分利用生物医药产业公共服务平台的优势,为高校、科研院所及企业提供技术咨询和检测服务。四是在司法鉴定服务方面,以提供DNA亲权鉴定业务为主。
目前,基因检测可分为四大检测板块:肿瘤易感基因、慢性病遗传病基因、产前与母婴诊断,以及各类包括健康管理和天赋基因的综合类检测。主要应用于医疗领域,且主要集中在生殖健康和肿瘤诊断及治疗两个领域。无创产前筛查是中国首个获批应用于临床的二代测序产品,也是基因行业是最成熟的一环;而肿瘤诊断及治疗被认为是下一个蓝海,企业争相布局。
以一个比较成熟的市场产业链为例,《中国基因测序行业市场前瞻与投资战略规划报告》(数据来源参考)表明:随着二孩政策放开,高龄高危孕产妇比例明显增高,加上无创产前基因检测应用范围和检测范围的扩大,无创产前基因检测市场就有望在未来几年达到百亿元以上。
国内基因行业的龙头企业,布局了基因测序全产业链,包括上游的测序仪及试剂、中下游的基因测序服务提供,并在无创产检、PGS/PGD、肿瘤诊断及治疗、伴随诊断等方面有优势。
2018年末,医院按等级分:三级医院1192个(其中:三甲医院722个),二级医院6780个,一级医院4989个,未评定等级医院6751个。目前全国几乎所有中大型医院都有对CNV检测的需求,这涉及所有的临床学科,绝大部分医院不能自行开展这些检测,必须委托第三方诊断公司。从有关报导来看,开展CNV的检测项目的,目前为止基本由贝瑞公司在做,但规模并不大。
健康管理和天赋基因的综合类检测,其针对目标为健康或亚健康人群,以较低廉的价格让消费者对自己的基因遗传情况以及患病可能有一定了解,这是市面上大众接触最多的一种类型。但这一类娱乐化较重,其专业性和医疗价值比较难以衡量,在专业性提升后潜力巨大。了解家族历史、遗传疾病潜在风险,更好地规划生活、规范行为,这一需求促使着直接面向顾客(direct
to consumer, DTC)类测序服务飞速发展,数以百万计的消费者成为生物技术公司的客户群,这背后的巨大市场也引入了企业和资本的涌入。
2019年05月30日,世纪经济报道,直接面向顾客(DTC)是我国的主流模式,指在没有医疗人员参与的情况下,直接向消费者销售的体外诊断产品模式。消费级DTC基因检测产品的消费全流程一般包括五步:购买检测、绑定账号、唾液采样、回寄试管、查看报告。2016年参与消费级基因检测并拥有自身数据的个人用户总量约为10万人,2017年约为30万人。目前,中国消费级基因检测服务的人口渗透率是0.03%,也就是说在2022年,中国将有5000万人拥有自己的基因组数据,市场空间巨大。
因此,开发基因组拷贝数目变异(CNV)临床检测应用具有互补性的项目,不仅可以填补国内的市场需求,而且,也是未来基因诊断行业的发展方向所在。
国内主要基因公司及医学独立实验室企业简介
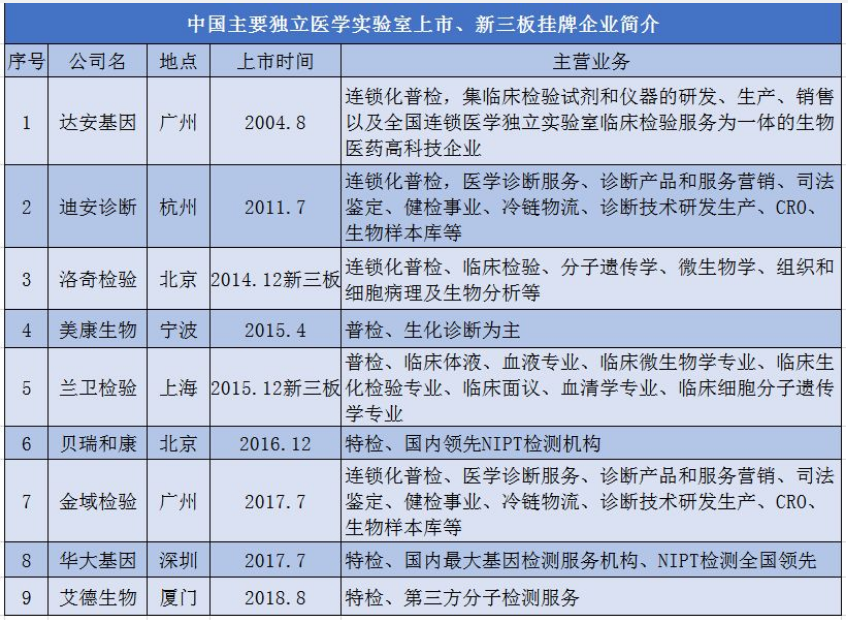
传统意义上的无创产前基因检测(NIPT)
传统意义上的无创产前基因检测(NIPT),这在我国有很大的市场需求。仅2016年我国已完成了上百万例临床样本的检测。但根据国家卫计委在2014年已经批准开展的无创产前基因检测,主要针对的是包括唐氏综合征在内的三种染色体疾病而已,并非基因检测。像国内知名的华大基因,早在2014年推出了首个基于高通量测序技术针对夫妻双方在怀孕前或孕早期基因检测服务-康孕,这能够检测近600种单基因疾病,但价格并未公开。而在华大基因提供的其他孕期检测项目里,如“孕因宝”,这一通过唾液检测夫妻遗传病基因的服务,能够检测69种常见遗传病基因,价格为3500元。香港地区做这类产前遗传病基因测试,价格约为4,500至8,000港元。
以一个比较成熟的市场产业链为例,《中国基因测序行业市场前瞻与投资战略规划报告》(数据来源参考)表明:随着二孩政策放开,高龄高危孕产妇比例明显增高,加上无创产前基因检测应用范围和检测范围的扩大,无创产前基因检测市场就有望在未来几年达到百亿元以上。
目前开展CNV检测业务的基因公司
目前,在全国十大基因公司中,开展CNV检测业务的有三家,即:贝瑞和康,安诺优达,华大基因。三家公司的业务局限于产前诊断。
贝瑞和康
(贝全安-WES+CNV-Seq服务套餐)
针对如智力障碍、发育迟缓儿童及因胎儿结构异常引发的流产物,建议进行全外显子组测序(WES)及低深度全基因组测序检测CNV-seq,同时检测单碱基变异及染色体畸变,提高临床诊断率。
哪些人可以选择贝全安-WES+CNV-Seq:
1. 染色体核型分析正常,但临床表现为发育迟缓、智力低下、各种畸形、生育障碍等的患儿及其父母;
2. 发生反复流产,需要查明原因的家庭;
3. 超声显示胎儿结构异常、停育等流产。
安诺优达
(低覆盖度CNV检测)
安诺低覆盖度CNV检测的分析条目:
1. 染色体倍性变异和CNV检测;
2. 染色体倍性变异和CNV全染色体模拟图;
3. 染色体倍性变异和CNV注释。
可检测变异种类:
1. 拷贝数变异(分辨率~100
kb);
2. 非整倍体异常;
3. 多倍体异常(69,
XXY);
4. 嵌合体。
华大基因:
1.华大基因康孕-染色体检测-100K
(CNV-seq),通过对受检样本提取DNA,如胚胎绒毛组织、胎儿组织、外周血等,采用高通量测序技术检测23对染色体非整倍体变异、100Kb以上的缺失、重复,可用于排查自然流产、先天畸形、智力障碍、发育迟缓等疾病的遗传病因。
2. 康孕-染色体检测-100K
(CNV-seq) 的有效数据量高达35M
reads,相比低数据量而言,可带来更准确的检测结果,不仅可以减少假阳性带来的临床决策偏差,还可以有效降低假阴性导致的漏检发生,真正做到对临床负责,对受检者负责。
3. 中信湘雅生殖与遗传专科医院与深圳华大基因研究院合作建立了一种基于全基因组低覆盖度测序,从单细胞水平检测拷贝数变异(CNV)的信息分析方法(简称单细胞CNV方法),并将该技术回顾性分析了38个胚胎滋养层细胞。经过研究,科研人员发现该方法具有更高的特异性及灵敏性,未来可大力辅助生殖临床应用检测。
刚需产品调研及非刚需产品调研
刚需产品调研
中国主流基因测序公司的人类医学产品大类包括,辅助生殖、孕妇产前、新生儿检测、单基因病检测、肿瘤个体化治疗、遗传性肿瘤预测、肿瘤早期筛查等。
调研显示,辅助生殖、孕妇产前、肿瘤个体化治疗和肿瘤早期筛查产品的市场接受程度较高;而消费者为新生儿、单基因病、遗传性肿瘤预测等检测项目买单的意愿较低。(21世纪经济,2014)
产品线具体分析如下:
1、辅助生殖基因检测(刚需):
即通常所说的试管婴儿。但目前辅助生殖基因检测只能检测受精卵的染色体数目是否异常,可以筛查的疾病包括唐氏综合征等少量与染色体相关的疾病。准父母更加需要全基因组检测,以便事先获知其他疾病的发生几率,如癌症、心血管疾病等。
中华实用儿科临床杂志『2017,32(12)』报导:不明原因智力障碍64例全基因组拷贝数变异分析,64例智力障碍患儿中16例检出CNVs,检出率为25%。16例CNVs中,6例微缺失/微重复片段<5Mb,最小检出缺失片段0.53Mb,这在常规染色体核型分析中是无法检出的。
2、孕妇产前检测(刚需):
孕妇产前基因检测可代替羊水穿刺手段检测胎儿是否患有唐氏综合征等染色体疾病(T21,T18,T13),对于唐筛高危和高龄孕妇而言属于刚需产品。无创产前检测已成为基因公司医学部门的主要收入来源,市场前景广阔,竞争激烈。
以产前诊断为例,CNV技术具有通量高,成本低,实验操作简便,检测分辨率高,临床应用成熟稳定等特点,在一定程度上彻底改变了中国产前诊断供给不足的局面。使得中国产前诊断的核心痛点逐渐从“供给不足”转移到“遗传咨询能力不足”的问题上来了。http://www.seqchina.cn/10733.html
3、肿瘤个体化治疗检测(准刚需):
在罹患肿瘤后,通过肿瘤相关基因检测可以使治疗、用药更加有针对性,并减少患者痛苦,以及延长生存期。但由于并不能保证治愈,所以这类检测归为准刚需产品。
目前推出的肿瘤个体化治疗基因检测既包括针对具体肿瘤的检测,又包括肿瘤相关全部基因检测,产品较为有效成熟。
患者进行此类检测,还可节省在身体上的试错性治疗,只需多花万元多的检测费用(全相关检测),故无论是患者还是患者家属均存在较大的意愿。
4、肿瘤早期筛查(准刚需):
由于近年来罹患肿瘤的比例逐渐增加,肿瘤早期筛查受到中等以上收入群体的青睐,在经济条件许可的条件下,大多数消费者愿意每年进行早期肿瘤筛查,以便治愈。事实上,即使低收入群体,也十分愿意在感觉不良时筛查是否罹患肿瘤。
调研对象给出的心理价位在3000-6000元/年。但令人遗憾的是,除了虚假或夸大宣传外,目前没有基因公司可以提供精确度极高的早期肿瘤筛查检测,原因是样本人群尚未积累足够大,另外,对血液中游离的微量肿瘤DNA残片没有十分精确的检测方法。
非刚需产品调研
1、新生儿基因检测(非刚需):
新生儿基因检测的内容各公司存在差异,但大多包括常见的遗传性疾病,如地中海贫血、罕见病、新生儿耳聋等。但这些遗传性疾病中的大多数尚无成熟的治疗手段,仅有个别病种可提前干预,故新生儿基因检测属于非刚需产品。
接受采访的家长们称,知道孩子可能会罹患某种疾病,但也只是知道概率,并且现阶段医学难以治愈或预防,在经济条件允许的情况下可以检测;还有一部分受访者认为,只能提出问题,不能解决问题,还是不知道的好。
2、单基因病检测(非刚需):
单基因病,顾名思义是由单一基因引发的疾病,包括心脏系统、神经系统疾病等,如心源性猝死、肥厚型心肌病、帕金森综合症、阿尔茨海默病等。
由于单基因病检测是一种易发性疾病的预测,并且没有有效科学的预防手段,此类检测属于非刚需产品,虽然那些家族中存在猝死先例的个体有望尝试此类检测。
3、遗传性肿瘤预测检测(非刚需):
此类基因检测针对那些家族中有患病先例的个体,包括十余种有遗传性的肿瘤,如乳腺癌、卵巢癌、肺癌、肾癌、胃癌等。携带一些特定易感基因的个体比常人更容易罹患肿瘤。
但由于只能提出问题而不能解决问题,即在知道自己更易罹患某种疾病后,并无有效手段加以预防。一个例外的例子是乳腺癌,可以通过切除腺体预防疾病发生,但肺癌、胃癌、肾癌等的预防并不能靠切除的方法。故遗传性肿瘤预测检测属于非刚需产品,仍存在较大比例的中国公众宁愿不知道结果。
国际肿瘤学杂志(2012年8月第39卷第8期)综述报导:CNV如果发生在肿瘤相关基因序列内部或周围可能引起癌基因激活、抑癌基因失活,最终导致肿瘤的发生。CNV通过改变基因剂量、调节基因活性影响基因表达、表型差异和表型适应,从而引起肿瘤以及其他遗传疾病。研究CNV对于探索染色体重组、基因组进化、基因表达以及多种复杂疾病尤其是肿瘤的发病机制有很大帮助。
在相关检测技术快速发展的推动下,人们已经发现了诸多与各类疾病发生密切相关的拷贝数变异。当前人们对拷贝数变异与疾病关系的认识主要集中于发育疾病、感染与免疫疾病、神经系统疾病以及各类肿瘤。
随着中国相关诊断供给能力的提升,大规模相关诊断临床实践经验和中国CNV大数据的积累必定会大大推动中国相关临床学科诊断依据和治疗方案能力的提升。
2.拟开展的CNV和基因变异检测项目
神经系统疾病:
普拉德-威利_天使症候群(Parder-Willi
Angelman syndrome)甲基化特异性多重连接探针扩增及甲基化特异性分析
脊髓性肌萎缩症及相关疾病SMA-SMN1和SMN2基因剂量诊断分析
结节性硬化症的TSC基因拷贝数目分析
杜显氏/贝克氏肌肉萎缩症(DMD-BMD)基因拷贝数目分析
儿童自闭症、发育障碍、癫痫相关的大区域片段基因拷贝数目变异分析
中枢神经系统疾病发育不良,包括乔伯特综合症,先天性肌营养不良症,少年肌萎缩性侧索硬化,周期性麻痹,肌强直、桥小脑发育不全,大头小头畸形,脑白质营养不良,
遗传性痉挛性截瘫,
肌张力障碍和帕金森症等疾病基因分析
先天性低钾症评估
遗传性原发性运动感觉性神经病(含Charcot-Marie-Tooth病
夏科-马里-图思病)基因诊断
线粒体与代谢疾病:
线粒体基因大片段缺失分析
线粒体脑病/Leigh
Syndrome核基因分析
进行性眼外肌麻痹(PEO)/视神经萎缩核基因分析
新生儿代谢病
肿瘤:
乳腺癌BRCA1/BRCA2基因变异与大片段缺失与重复分析
结直肠癌和LYNCH综合征风险基因分析
遗传性胰腺癌基因变异分析
肿瘤相关50个基因的全面分析
肾癌相关基因分析
遗传性MDS/白血病基因突变与染色体易位分析
肿瘤单基因分析(TP53,
PTEN, RET, PTCH1, STK11, VHL, FH, FLCN, PRKAR1A, MEN1, CDC73等等
儿童相关肿瘤基因分析
脑部肿瘤相关基因拷贝数目分析
甲状旁腺功能亢进/内分泌肿瘤基因分析
心血管疾病:
肥厚性与扩张型心肌病(HCM)基因分析
突发型心脏骤停性心律不齐
儿茶酚胺能性多动性室性心动过速
心律失常性右室心肌病
斯蒂克勒综合症
马凡综合征TAAD
家族性高胆固醇血症
Holt-Oram综合征(TBX5)
因子V莱顿血友病
长QT综合征LQTS
其他罕见疾病:
性器官发育与性别反转基因检测
男性不育症AZT
遗传性多囊肾多囊肝
远端肾小管性酸中毒
肾结石症和肾钙化病
神经性耳聋STRC
免疫缺陷疾病包括自身免疫性淋巴组织增生综合征,
IRAK4缺陷,重症联合免疫缺陷病(
SCID )
骨骼发育不良
罗宾诺综合症
采用WGS和基因芯片技术对疾病相关的多种大区域CNV进行检测,覆盖数百种包括下列已知的病理性大片段CNV。同时对未知和新发现的千百种CNV进行检测和意义评估。
已知的病理性:
10q11.2
recurrent region (LCR-C to -D)
10q22.3q23.2
recurrent region (LCR-3/4-flanked) (includes BMPR1A)
11p11.2
(Potocki-Shaffer syndrome) region (includes ALX4, EXT2)
11p13
(WAGR syndrome) region
11q13.2q13.4
recurrent region (includes SHANK2, FGFs)
14q11.2
region (TCRA region)
14q11.2
region including CHD8 and SUPT16H
14q32
region associated with UPD(14) phenotypes
15q11.2
recurrent region (BP1-BP2) (includes NIPA1)
15q11q13
recurrent (PWS/AS) region (BP1-BP3, Class 1)
15q11q13
recurrent (PWS/AS) region (BP2-BP3, Class 2)
15q13.3
recurrent region (BP4-BP5) (includes CHRNA7)
15q13.3
recurrent region (D-CHRNA7 to BP5) (includes CHRNA7 and OTUD7A)
15q24
recurrent region (A-D) (includes SIN3A)
15q25.2
recurrent region (LCR B-C, proximal)
16p11.2
recurrent region (includes SH2B1) (distal region) (BP2-BP3)
16p11.2
recurrent region (includes TBX6) (proximal region) (BP4-BP5)
16p12.2
recurrent region (includes EEF2K, CDR2)
16p13.11
recurrent region (includes MYH11)
16p13.3
region (includes CREBBP)
17p11.2
recurrent (SMS/PLS) region (includes RAI1)
17p12
recurrent (HNPP/CMT1A) region (includes PMP22)
17p13.3
(Miller-Dieker syndrome) region (includes YWHAE and PAFAH1B1)
17q11.2
recurrent region (includes NF1)
17q12
recurrent (RCAD syndrome) region (includes HNF1B)
17q21.3
recurrent region (includes KANSL1)
19q13.3
region (PSG gene cluster)
1p36
terminal region (includes GABRD)
1q21.1
recurrent (TAR syndrome) region (BP2-BP3, proximal) (includes RBM8A)
1q21.1
recurrent region (BP3-BP4, distal) (includes GJA5)
1q21.2
region (polymorphic region)
1q43q44
terminal region (includes AKT3)
22q11.2
recurrent (DGS/VCFS) region (proximal, A-B) (includes TBX1)
22q11.2
recurrent (DGS/VCFS) region (proximal, A-D) (includes TBX1)
22q11.2
recurrent region (central, B/C-D) (includes CRKL)
22q11.2
recurrent region (distal type I, D-E/F)
22q11.2
recurrent region (distal type II, E-F)
22q11.21
recurrent (Cat eye syndrome) region (includes CECR2)
2p15p16.1
region (includes BCL11A)
2p21
region (includes PREPL and SLC3A1)
2p24.3
MYCN-DDX1 duplication region
2q11.2
recurrent region (ARID5A, LMAN2L included)
2q13
recurrent region (includes BCL2L11)
2q13
recurrent region (includes NPHP1)
2q21.1
recurrent region (includes ARHGEF4, GPR148)
2q37.3
terminal region (includes HDAC4)
3q29
recurrent region (includes DLG1)
4p16.3
terminal (Wolf-Hirshhorn syndrome) region
5p15
terminal (Cri du chat syndrome) region
5q35
recurrent (Sotos syndrome) region (includes NSD1)
6q24
region (includes PLAGL1)
7q11.23
recurrent (Williams-Beuren syndrome) region (includes ELN)
7q36.3
ZRS (SHH cis-regulatory) duplication region (within LMBR1 intron 5)
8p23.1
recurrent region (includes GATA4)
8p23.1
region (DEFB gene cluster)
DLK1-MEG3
Intergenic DMR
Xp11.22p11.23
recurrent region (includes SHROOM4)
Xp11.23
region (includes MAOA and MAOB)
Xp22.31
recurrent region (includes STS)
Xq28
recurrent region (includes GDI1)
Xq28 recurrent region
(int22h1/int22h2-flanked) (includes RAB39B)
3.项目核心团队人员简历
医学博士 教授
项目创始人
人类疾病基因学专家
毕业于中南大学湘雅医学院医疗系和解放军总医院军医进修学院;从事临床医学、遗传学与肿瘤研究十多年;先后在美国乔治城大学、纽约医学中心、美国三大基因检验公司中的QUEST和BIOREFERENCE从事人类疾病基因学研究和诊断工作近二十年;在美国BIOREFERENCE公司担任基因组拷贝数目变异(CNV)项目首席科学家及该项目研究团队负责人五年;率先开展了该CNV项目的全球(主要是殴美发达国家)最具学术前沿的诊断业务,学术成果发表在美国遗传学杂志等国际学术期刊上,拥有非常丰富的人类疾病基因学的知识和经验。
1979年 中南大学湘雅医学院医疗系
1990年 解放军总医院军医进修学院硕士
1995年 解放军总医院军医进修学院博士
2000年 美国乔治城大学博士后
2001年 解放军总医院副主任医师,副教授,硕士生导师
2002年 美国乔治城大学遗传与肿瘤研究所
2010年 美国纽约Downstate医学中心
2013年 美国Quest诊断公司
2014年-美国Bioreference基因诊断公司,CNV项目首席科学家及项目负责人
毕业于中南大学湘雅医学院医疗系和美国EMORY大学;先后从事国家卫生部、世界卫生组织(WHO)、世界银行(WORLDBANK)、美国疾病控制中心(CDC)大型健康项目研究和管理工作十多年;在国际大型金融集团的美国大都会保险公司(METLIFE)、加拿大明信理财集团(CLARICA)和永明金融集团(SUNLIFE)工作二十年;拥有丰富的健康项目管理、基金、保险、税务、投资等专业工作经验。主要获奖:联合国开发计划署项目管理研究成果奖;美国大都会保险公司成就奖;加拿大明信理财集团优秀奖。
1979年 中南大学湘雅医学院医疗系
1985年 国家卫生部,疾病控制项目管理
(主任科员;医师;主管长江以南十一省市自治区的疾病控制规划与项目)
1988年 世界卫生组织(WHO)亚太办事处(菲律宾马尼拉)项目管理
(世界卫生组织WHO卫生管理规划工作一年;熟悉WHO项目规划)
1991年 日本,巴西,菲律宾流行病学项目管理课题研究
(世界卫生组织WHO发达国家与发展中国家的公共卫生与健康研究项目)
1992年 世界银行疾病控制项目管理
(四亿美元项目主管之一;掌握世界银行全套大型项目运作管理经验)
1993年 美国Emory大学,公共卫生和健康管理(硕士)
(注:Emory大学国际卫生专业在美国排名第一)
1996年 美国疾病控制中心(CDC),热带病控制项目研究和管理
(熟悉美国疾病控制中心CDC疾病控制项目运作管理模式)
1997年--2016 年分别在美国大都会保险公司(METLIFE),加拿大明信理财集团(CLARICA),加拿大永明理财集团(SUNLIFE)工作,学习了大量的金融和投资知识,掌握了从企业到个人的理财规划和投资的技能,拥有基金、保险、投资的相关专业证书,熟悉北美相关大型金融机构的企业文化与市场运作模式;北美企业、投资、财经和税务体系/领域经验非富。
临床医学博士 教授 项目创始人 临床分子遗传疾病医学专家
毕业于中南大学湘雅医学院医疗系和解放军总医院军医进修学院;主任医师;临床医学研究生导师;教授;从事临床医学三十多年;先后在中南大学湘雅医学院附二医院、中国人民解放军总医学、老年心血管病研究所和救治中心、美国乔治城大学医学中心、新泽西医学中心、美国首都华盛顿医学中心等世界著名医疗机构从事内科疑难疾病、分子遗传疾病、心血管疾病临床工作、科研、教学;具有丰富的临床疑难疾病、分子遗传疾病的诊断经验,并进行了多项相关课题的研究,多项研究成果发表在一流的生物医学杂志。
高级经济师 项目合伙人 企业财务管理专家
毕业于湖南财经学院;1993年开始从事投资银行工作;先后任职于北京京华信托、大鹏证券、国元证券、湘财证券、中山证券、五矿证券等单位;全国首届经济师获得者,通过首届证券投行从业资格考试;主持山东浪潮、山东电缆、鲁银投资、正虹科技、银山化工等公司IPO上市业务;对企业上市、并购重组、财务顾问等业务具有丰富的实际操作经验。
数十年来,主要从事企业管理、企业投资融资、企业上市、投资基金等工作经验。
主导和指导了二十多家企业成功上市
。
1984 湖南大学财经学院
1993- 深圳证券公司投资银行部,投资基金
4.深圳政府有关促进企业发展的政策支持
《关于促进科技创新的若干措施》节选:
*鼓励海外高层次人才创新创业团队发起设立专业性、公益性、开放性的新型研发机构,予以最高1亿元支持。
*推动转制科研院所、高新技术企业、科技服务型企业实施管理层和核心骨干持股,持股比例上限放宽至30%。
《关于促进人才优先发展的若干措施》节选
*经评审认定的海外高层次人才“团队+项目”,给予最高1亿元资助。
*出国留学人员来深创业,符合条件的给予30万元-100万元创业资助,特别优秀项目给予最高500万元资助。
*对符合条件的创客个人、创客团队项目给予最高100万元资助。
*支持境外机构在深圳设立具有独立法人资格、符合我市产业发展需求的技术转移机构,政府给予最高1000万元研发资助。
*2016年-2020年期间,深圳将新筹集不少于30万套人才住房。
《深圳市鼓励总部企业发展暂行办法》节选
*经认定的总部企业,认定当年给予落户奖励1000万元。
*自认定年度第三年起可以提出申请贡献奖。奖励额为上一年度形成本市地方财力超过其自认定为总部企业年度以来历史最高值的30%,最高不超过2000万元。奖励资金应当用于在本市企业的技术研发、品牌推广、市场拓展和人力资源开发。
*在本市无自有办公用房的,自认定之日起3年内,租用总部自用办公用房(不包括附属设施和配套用房)的,每年按每平方米500元的标准给予补助,每年补助金额不超过150万元。
*在本市无自有办公用房的,自认定之日起3年内,购置总部自用办公用房(不包括附属设施和配套用房)的,按购房房价5%的标准给予一次性补助。
《深圳生物产业振兴发展政策》节选
*在深圳设立符合规定条件的研发中心、工程实验室、重点实验室、工程中心、公共技术服务平台,专项资金予以最高500万元资助。
*对自主创新生物产品研发,专项资金予以最高800万元资助。
*生物企业申请美国FDA认证、欧盟cGMP和CE认证、世界卫生组织认证及其他国际市场准入认证,开展生物产品国际多中心临床研究或申请国外注册,专项资金予以最高800万元资助。
*经认定的生物企业入驻政府投资建设的创新型产业用房,首3年予以500平方米以下部分免房租、500-1000平方米部分房租减半资助。
*对属于产业发展重点领域且为产业链缺失环节的产业化项目,专项资金予以最高500万元资助。
*专项资金每年安排不低于500万元,用于资助在深圳举办中国国际医疗器械博览会等生物产业展会,深圳生物企业参加全国药品交易会、德国国际医院及医疗设备展览会(MEDICA)等境内外生物产业专业展会。
《深圳市未来产业发展政策》节选
(生命健康、海洋、航空航天等产业)
*在深圳设立符合规定条件的市级工程实验室、重点实验室、工程(技术)研究中心、企业技术中心,专项资金予以最高500万元支持。
*对开放式、专业化共性技术服务平台建设,专项资金予以最高500万元支持。
*企业申请并获得国内外市场准入认证的,专项资金予以最高500万元支持。
*专项资金每年安排不低于1000万元,用于支持深圳企业参加未来产业领域国内外知名展会,以及在深圳举办高水平的国际性展会。
参考:我们关注的基因测序领域重点公司
华大基因:国内基因测序龙头,业务全面丰富
华大基因是国内基因测序方面历史最悠久,收入规模最大、业务最全面的龙头企业之一。华大基因的主营业务为通过基因检测等手段,为医疗机构、科研机构、企事业单位等提供基因组学类的诊断和研究服务。
其业务主要有生育健康基础研究和临床应用服务、基础科学研究服务、复杂疾病基础研究和临床应用服务、药物基础研究和临床应用服务等,业务涵盖从基础研究到前沿应用的广阔领域。同时,2013年公司控股股东华大控股收购了美国研发基因测序仪的上市公司CompleteGenomics,为公司提供了自主测序平台及相关技术。
公司总部位于中国深圳,在北京、天津、武汉、上海、广州等国内主要城市设有分支机构和医学检验所,并在香港、欧洲、美洲、亚太等地区设有海外中心和核心实验室,已形成「覆盖全国、辐射全球」的网络布局。
2016年,公司实现营业收入17.1亿元。
贝瑞和康:NIPT业务有特色有实力,产品+服务双线推进
贝瑞和康主营业务为以测序为基础的基因检测服务与设备试剂销售,公司致力于基因测序技术在医学临床领域的转化与应用,提供「无创式」基因检测项目。依托高通量测序分子诊断平台,凭借自主研发的核心技术,构建覆盖生育健康、肿瘤分子检测与诊断的多层次产品及服务体系。
公司业务主要分为两大类:面向医院及第三方医学实验室的医学产品及服务,以及面向科研高校院所的基于高通量测序的基础科研服务。报告期内,公司覆盖的NIPT检测样本数达59.5万例,医学检验收入8.78亿元,公司NIPT业务在国内有较强影响力,既能为医疗机构提供NIPT检测服务,又能以产品形式提供测序仪及试剂盒,适应不同级别医疗机构的不同需求。2016年,试剂销售和设备销售合计收入占主营业务收入的比重达到30.56%。
公司总部位于北京,在北京、上海、青岛、成都设有4个检验所,并在香港设有子公司。贝瑞和康通过杭州贝瑞进行测序仪和试剂生产,并通过北京贝瑞进行销售,与多家医院合作共建实验室,逐步建立覆盖全国的渠道网络。
2016年,公司实现营业收入9.2亿元。
鵾远基因:甲基化高通量测序技术领先,肿瘤基因组学领域优秀企业
鵾远基因(SingleraGenomics)由知名华人科学家高远教授(约翰霍普金斯大学),张鵾教授(加州大学圣地亚哥分校)联合其他创始人CEO张江立、COO刘强、CTO刘蕊博士共同组建。
位于中国上海及美国加州圣地亚哥的鵾远基因公司,在单细胞测序、DNA甲基化测序以及生物信息学方面拥有独有的专利技术;公司主要产品服务包括肿瘤诊断及个性化治疗、无创产前诊断等;公司致力于发展精准医疗,努力为病人提供早期、精准的诊疗信息。目前产品包括肿瘤热点突变和药物代谢基因检测、肺癌RNA融合基因检测、BRAC1、BRAC2遗传突变检测、外周血样本肿瘤ctDNA检测等。
我们认为公司在甲基化测序和生物信息学方面有自己的特色和领先性,公司在肿瘤早期诊断方面具有一定优势,不仅能以较高灵敏度捕获和检测血液肿瘤中的ctDNA片段,还能通过甲基化信息指示其组织来源,为寻找肿瘤原发灶提供帮助,这对于ctDNA液体活检的临床使用化具有重大意义。
公司与复旦大学泰州健康科学研究院签署精准医疗战略合作协议,在合作中鵾远基因将利用自己的专利单细胞测序技术和甲基化靶向测序技术以及其他国际领先的NGS测序技术专利与复旦泰州研究院共同开展20万人大型人群队列中常见恶性肿瘤的跟踪随访工作,力求在多个癌种中开发出高特异度和灵敏度的早期无创检测方法,从而建立癌症风险评估、预防和早期筛查的系统解决方案
2016年8月22日,鵾远基因宣布成功完成2000万美金的A轮融资。
博圣生物:全国性的出生缺陷防控综合服务商
杭州博圣生物技术有限公司是提供出生缺陷防控一站式综合解决方案的专业机构,专注于提供产前筛查、产前诊断、新生儿遗传代谢病筛查,遗传诊断等项目的技术与服务。
博圣生物搭建了完整的免疫学筛查技术、基因晶片技术、高通量基因测序技术和串联质谱技术等多层次技术平台,专注为国内出生缺陷防控领域客户提供筛查与诊治、产品与服务、培训与公益救助的一体化解决方案,是优生遗传领域的行业先行者和引领者,近年经营业绩一直呈现30%以上的年均增长速度。
目前,博圣每年的检测量达到3500万人份,每年避免超过1万名出生缺陷患儿的社会负担。2016年,公司的销售额预计超过7亿元。
2015年1月8日,迪安诊断出资23252万元受让博圣生物的25%股权。
2016年9月,迪安诊断全资子公司杭州意峥向博圣生物增资12,000万元,并以6000万元受让博圣生物增资后4%股权。完成上述增资及股权转让后,杭州意峥和迪安诊断共持有博圣生物35%股权,博圣生物业绩承诺为2015年□利润不低于10140万元、2016年□利润不低于13182万元、2017年□利润不低于17136.6万元。
燃石医学:肿瘤基因组学转化先锋
燃石医学成立于2014年3月,总部位于北京,其第一家医学检验所位于广州,随后在上海建立了研发中心,总占地面积10000多平方米。燃石医学专注于肿瘤患者个体化治疗指导,以二代测序及医学生物信息学为核心,常规肿瘤分子病理检测为基石,致力于打造肿瘤个体化治疗临床检测服务及科研一站式解决方案。燃石医学更是唯一一家拥有临床医学部的第三方临床检验机构。
公司先后开发了肺癌靶向药检测Panel,甲状腺癌良恶性判断检测Panel,肺癌液体活检基因检测Panel,以及多癌种的遗传易感基因检测Panel。当前产品涵盖肿瘤个体化基因检测、肿瘤个体化液体活检、遗传性肿瘤检测、良恶性判断等领域。
2017年2月16日,燃石医学-CTONG联合实验室顺利通过美国卫生及公共服务部(HHS)医疗保险及医疗补助服务中心(CMS)审查,获得美国临床实验室改进法案修正案(CLIA)认证证书,成为中国第一间(也是目前唯一)获得美国CLIA认证的ctDNA和肿瘤组织二代测序(NGS)临床检测实验室。
2016年12月28日,燃石医学宣布完成总额为3亿元的B轮融资。此前,燃石医学已完成两轮融资,分别为2014年A轮4,300万元和2015年A+轮1.5亿元。
安诺优达:科技服务+产前诊断+肿瘤基因检测三线发展
安诺优达基因科技成立于2012年,总部位于北京,专注于新一代基因组学技术在人类医学健康和生命科学研究两大领域的产业化应用,业务涵盖胎儿产前检测、胚胎植入前遗传学检测、液体活检、肿瘤基因检测、血液病基因检测等多个领域。
在科技服务领域,安诺基因作为安诺优达旗下注册品牌,在基因组学、转录组学和表观遗传学等多组学水平与国内外高校院所和研发机构广泛开展科研合作,涉及领域包括人类重大疾病基础研究、动植物分子育种、遗传与进化、环境微生物和生态等。
公司已经在已在生育生殖健康、肿瘤个性化诊疗和基因体检几大方向形成了优秀的产品体系和品牌效应,推出了包括无创产前DNA检测、ctDNA检测、NGS肿瘤个体化用药指导基因检测、血液病基因检测、乳腺癌/卵巢癌基因检测在内的一批优秀的高通量测序临床应用项目。
2017年3月21日,安诺优达在北京召开新产品发布会,正式推出近日获得中国食品药品监督管理总局(CFDA)注册认证的新款桌面式高通量基因测序仪NextSeq550AR,该测序仪是Illumina公司与安诺优达合作开发的新一代桌面式高通量基因测序仪,主要用于产前检测,具备极强的临床和学术应用延展性,包括PGS、液体活检、FFPE测序、遗传病检测等都可以在此测序平台上进行试剂盒的开发和注册。
世和基因:肿瘤基因检测标的,北陆药业参股企业
世和基因是癌症个体化医疗诊断领域的优秀企业,世和基因北美总部坐落在加拿大多伦多,中国总部落户于南京,此外世和在美国史丹福大学设有生物信息学分部。
世和基因产品主要包括全景癌症基因检测、健康人癌症预警检测、21基因表达预后及复发风险预测、视网膜母细胞瘤分子基因检测、科研合作项目等。2016年,公司推出针对血液系统肿瘤(包括淋巴瘤),结合DNA/mRNA高通量测序的检测产品──血默胜,对390个基因进行DNA测序检测,并结合全mRNA测序更加全面的反映基因融合和表达,是国内首个全面覆盖各类型血液系统肿瘤的检测产品。
A股上市北陆药业先后于2014年和2016年投资和增资世和基因共计6000万元,持有世和基因22.7273%的股权。公司公告指出,「世和基因拥有完全自主开发的高通量癌症基因富集提取、测序和生物信息学分析技术并处于国际领先地位。该项服务在国内拥有极高的技术门槛。」